��Ŀ����
����Ŀ�������Ǽס��ҡ�����λͬѧ��ȡ���������Ĺ��̣��������������ʵ���������ۣ� ��ʵ��Ŀ�ġ���ȡ��������
��ʵ��ԭ�����ס��ҡ�����λͬѧ����ȡ�Ҵ���������Ũ�����Ϲ��ȵķ�����ȡ����������
��װ����ơ��ס��ҡ�����λͬѧ�ֱ��������������ʵ��װ�ã�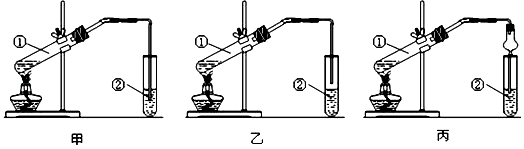
���ݷ����ش�
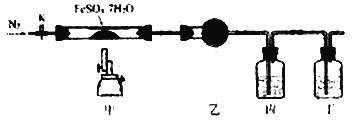
��1����λͬѧ��Ƶ�װ���������������ѡ��ס����ҡ���������ԭ���� ��
��2����ʵ�鲽�衿 a������ѡ���װ����װ���������Թܢ����ȼ���3mL�Ҵ�������ҡ���»�������2mLŨ������ҡ�ȣ���ȴ���ټ���2mL�����
b�����Թ̶ܹ�������̨�ϣ�
c�����Թܢ��м��������ı���Na2CO3��Һ��
d���þƾ��ƶ��Թܢټ��ȣ�
e�����۲쵽�Թܢ�������������ʱֹͣʵ�飮
�Թܢ��м���Ũ�����������
��3����ʵ���г����ܵ������� ��
��4���Թܢ��б���Na2CO3��Һ�����������ɷ���NaOH��Һ����Na2CO3��Һ������ǡ����������� ��
��5���Թܢ��й۲쵽�������������Թܢ��з��������������ʵ����������� ��
��6���ֱ�д���Թܢٺ͢��з�����Ӧ�Ļ�ѧ����ʽ ����
�� ��
���𰸡�
��1���ף�����������
��2����������ˮ��
��3����������
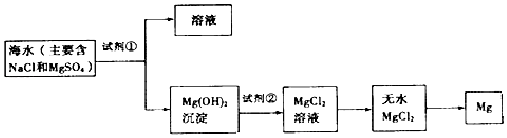
��4�������Ҵ�����ȥ������������������ܽ��,ʹ��ֲ��������� NaOH��ʹ��ˮ��
��5��Һ��ֲ㣻��Һ
��6��CH3COOH+C2H5OH ![]() CH3COOC2H5+H2O��2CH3COOH+Na2CO3�T2CH3COONa+H2O+CO2��
CH3COOC2H5+H2O��2CH3COOH+Na2CO3�T2CH3COONa+H2O+CO2��
���������⣺��װ����ơ���1��ʵ������ȡ���������ķ�Ӧ����������Ҵ���������Ҵ��ӷ���������Ҵ�������ˮ��������װ�����ҵ��ܲ�����Һ������Ϊ�˷�ֹ��������װ�����θ���ܵ�����ͬʱҲ���������ã���װ�õ��ܲ���Һ�����������������������
���Դ��ǣ��ף���������������ʵ�鲽�衿��2����ȡ���������ķ�ӦΪ���淴Ӧ��������ˮ���ɣ�Ũ��������ˮ�ԣ��ٽ��÷�Ӧ������Ӧ�����ƶ���Ũ�����ܼӿ췴Ӧ���ʣ�����Ũ��������������ˮ����
���Դ��ǣ���������ˮ���� ��3��������Ҵ��ӷ���װ���г����ܵ���Ҫ�����ǣ��������������������������ã�
���Դ��ǣ�������������4���Ʊ���������ʱ���ñ���̼������Һ��Ŀ�����кͻӷ����������ᣬʹ֮ת��Ϊ����������ˮ�У�������������������ζ���ܽ����ջӷ��������Ҵ�����������������ˮ�е��ܽ�ȣ����ڷֲ�õ�������������NaOH��Һ��Ӧ������������Ҳ����NaOH��Һ��Ӧ����ʹ��ˮ�������Ҵ��������ƣ������ϳ���ԭ�����Բ�����NaOH��Һ����Na2CO3��Һ��
���Դ��ǣ������Ҵ�����ȥ������������������ܽ�ȣ�ʹ��ֲ���������NaOH��ʹ��ˮ�⣻ ��5���������������ڱ���̼������Һ�������Թܢ��й۲쵽�������ǣ�Һ���Ϊ���㣨�ϲ�Ϊ��������Ϊ�������������ڱ���̼������Һ�����뻥������Һ��ķ����Ƿ�Һ�����Գ��÷�Һ������ʵ���е�����������
���Դ��ǣ�Һ��ֲ㣻��Һ����6����������Ӧ�ı���Ϊ�����ǻ��������⣬�������Ҵ���Ũ���������¼��ȷ���������Ӧ��������������ˮ���÷�ӦΪ���淴Ӧ����ѧ����ʽΪCH3COOH+C2H5OH ![]() CH3COOC2H5+H2O��
CH3COOC2H5+H2O��
���Դ��ǣ�CH3COOH+C2H5OH ![]() CH3COOC2H5+H2O��
CH3COOC2H5+H2O��
���Թܢ���̼���ƺ����ᷢ�����ֽⷴӦ����Ӧ����ʽΪ2CH3COOH+Na2CO3�T2CH3COONa+H2O+CO2����
���Դ��ǣ�2CH3COOH+Na2CO3�T2CH3COONa+H2O+CO2����

����Ŀ���й������ĸ����õ绯ѧװ�õ������У���ȷ���ǣ�������
|
|
|
|
ͼ�����п�̵�� | ͼ��Ǧ���������� | ͼ���⾫��ͭ | ͼ����пŦ�۵�� |
A.ͼ����ʾ����У�MnO2�������Ǵ���
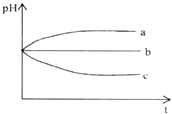
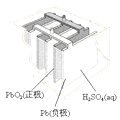
B.ͼII��ʾ��طŵ�����У�����Ũ�Ȳ�������
C.ͼIII��ʾװ�ù��������У��������Һ��Cu2+Ũ��ʼ�ղ���
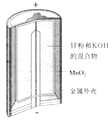
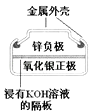
D.ͼIV��ʾ����У�Ag2O������������ع��������л�ԭΪAg