题目内容
某校化学研究性小组,利用下列提供的实验装置和试剂对某种燃煤所
含元素进行定性和定量检测,试回答:
(1)将燃煤充分燃烧,产生气体经化学分析主要含有CO2、H2O、SO2、N2四种气体,则该燃煤一定含有的元素为 .
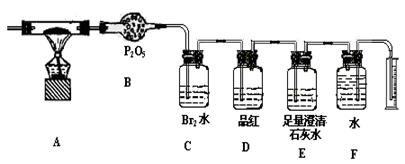
(2)称取该燃煤样品Wg,通入纯氧使其充分燃烧,检测该燃煤中所含上述元素的质量分数。利用下列装置进行实验:
①指出上述装置中B、C、D、E的作用
B C
D E
②为了准确测量F中收集到的气体体积并能根据实验时温度、压强计算其物质的量,正确的实验操作是
含元素进行定性和定量检测,试回答:

(1)将燃煤充分燃烧,产生气体经化学分析主要含有CO2、H2O、SO2、N2四种气体,则该燃煤一定含有的元素为 .
(2)称取该燃煤样品Wg,通入纯氧使其充分燃烧,检测该燃煤中所含上述元素的质量分数。利用下列装置进行实验:
①指出上述装置中B、C、D、E的作用
B C
D E
②为了准确测量F中收集到的气体体积并能根据实验时温度、压强计算其物质的量,正确的实验操作是
(1)C H S (2) ① 吸收水;吸收二氧化硫;检验二氧化硫是否吸收完全;检验二氧花碳 ②保持F中液面和量筒中液面处在相同高度,根据连通器原理排出液体体积为气体体积,F气体的气压和外界气压相同。
试题分析:(1)根据原子守恒可知,该燃煤中一定含有的元素是C、H、S。由于客气中含有氧气和氮气,所以氧元素和氮元素不能确定。
(2)①P2O5是一种干燥剂,所以B装置的主要作用是吸收水;溴水具有氧化性,而SO2具有还原性,所以C装置的作用是吸收二氧化硫;SO2能使品红溶液褪色,则装置D的作用是检验二氧化硫是否吸收完全;由于生成生物气体中还含有CO2,所以E中澄清石灰水的作用是检验二氧花碳。
②氮气不溶于水,所以F装置的作用是通过排水法测量氮气的体积,因此正确的实验操作是保持F中液面和量筒中液面处在相同高度,根据连通器原理排出液体体积为气体体积,F气体的气压和外界气压相同。
点评:该题是中等难度的试题,也是高考中的常见题型和考点。试题基础性强,侧重对学生实验分析、操作能力的培养,有利于培养学生的综合实验能力,提高学生分析问题,解决问题的能力。该题主要是以实验基本操作为中心,通过是什么、为什么和怎样做重点考查实验基本操作的规范性和准确性及灵活运用知识解决实际问题的能力。

练习册系列答案
相关题目

 R-Br+H2O ②
R-Br+H2O ②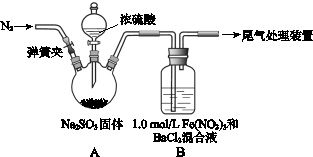
 【查阅资料】① 干燥的氯气在110℃~140℃与硫反应,即可得到S2C12。② S的熔点为112.8℃、沸点为444.6℃;S2C12的熔点为
【查阅资料】① 干燥的氯气在110℃~140℃与硫反应,即可得到S2C12。② S的熔点为112.8℃、沸点为444.6℃;S2C12的熔点为 76℃、沸点为138℃。
76℃、沸点为138℃。 2SCl2。④ S2C12易和水发生反应,生成H2S、SO2、H2SO3、H2SO4等。⑤ClO3-+5Cl-+6H
2SCl2。④ S2C12易和水发生反应,生成H2S、SO2、H2SO3、H2SO4等。⑤ClO3-+5Cl-+6H =3C12↑+3H2O 请回答下列问题:
=3C12↑+3H2O 请回答下列问题: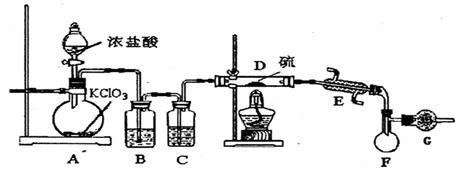
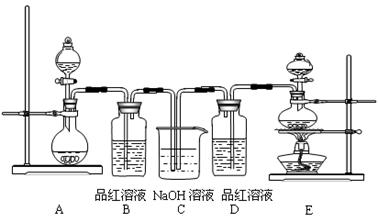
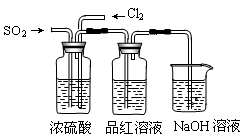
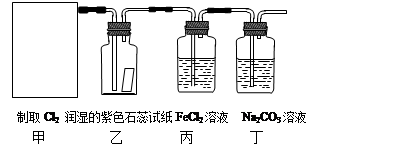
 MnCl2 + Cl2↑+ 2H2O。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质。
MnCl2 + Cl2↑+ 2H2O。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质。