题目内容
20.下列有关物质的应用与性质相一致的是( )| A. | SO2可用作漂白剂,原因是具有还原性 | |
| B. | FeCl3溶液可用于制印刷电路板,原因是能氧化Cu | |
| C. | Cl2可制漂白粉,原因是能与NaOH反应 | |
| D. | Al(OH)3可用于治疗胃酸过多,原因是碱性强 |
分析 A.二氧化硫可与有色物质化合生成无色物质;
B.Cu与氯化铁反应生成氯化铜、氯化亚铁;
C.漂白粉的成分为氯化钙、次氯酸钙;
D.氢氧化铝与盐酸反应,可中和胃酸.
解答 解:A.SO2可用作漂白剂,原因是二氧化硫与有色物质化合生成无色物质,与其还原性无关,故A错误;
B.Cu与氯化铁反应生成氯化铜、氯化亚铁,则FeCl3溶液可用于制印刷电路板,故B正确;
C.漂白粉的成分为氯化钙、次氯酸钙,则Cl2可制漂白粉,原因是能与石灰乳反应,故C错误;
D.氢氧化铝与盐酸反应,可中和胃酸,原因是氢氧化铝为不溶性的弱碱,故D错误;
故选B.
点评 本题考查物质的性质,为高频考点,综合考查元素化合物知识,把握物质的性质、发生的反应及性质与用途的关系为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案
相关题目
8.在测定中和热的实验中,下列说法正确的是( )
| A. | 使用环形玻璃搅拌棒是为了加快反应速率,使其充分反应,减小实验误差 | |
| B. | 为了准确测定反应混合溶液的温度,实验中温度计水银球应与小烧杯底部接触 | |
| C. | 为了使反应均匀进行,可以向酸(碱)中分次加入碱(酸) | |
| D. | 在测定中和热实验中需要使用的仪器有量筒、烧杯、胶头滴管、温度计等 |
5.下列各组的排列顺序中,正确的是( )
| A. | 原子半径 Na<Mg<Al | B. | 酸性 H2SiO3<H2CO3<H2SO4 | ||
| C. | 稳定性 HF<HCl<HBr | D. | 碱性 NaOH<Mg(OH)2<Al(OH)3 |
10.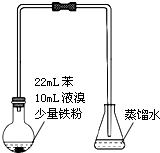 溴苯是不溶于水的液体,常温下不与酸、碱反应,可用如图装置制取(该反应放出热量).制取时观察到烧瓶中有大量红棕色蒸气,锥形瓶中导管口有白雾出现等现象.
溴苯是不溶于水的液体,常温下不与酸、碱反应,可用如图装置制取(该反应放出热量).制取时观察到烧瓶中有大量红棕色蒸气,锥形瓶中导管口有白雾出现等现象.
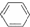 +Br2$\stackrel{铁屑}{→}$
+Br2$\stackrel{铁屑}{→}$ +HBr
+HBr
下列说法错误的是( )
 溴苯是不溶于水的液体,常温下不与酸、碱反应,可用如图装置制取(该反应放出热量).制取时观察到烧瓶中有大量红棕色蒸气,锥形瓶中导管口有白雾出现等现象.
溴苯是不溶于水的液体,常温下不与酸、碱反应,可用如图装置制取(该反应放出热量).制取时观察到烧瓶中有大量红棕色蒸气,锥形瓶中导管口有白雾出现等现象. +Br2$\stackrel{铁屑}{→}$
+Br2$\stackrel{铁屑}{→}$ +HBr
+HBr下列说法错误的是( )
| A. | 制备溴苯的反应属于取代反应 | |
| B. | 白雾出现是因为HBr易挥发且极易溶于水 | |
| C. | 装置图中长直玻璃导管仅起导气作用 | |
| D. | 溴苯中溶有少量的溴,可用NaOH溶液洗涤除去 |
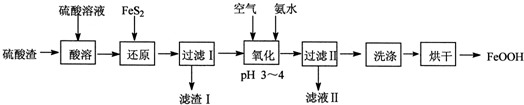
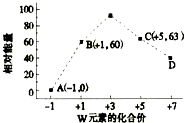 已知前四周期五种元素X、Y、Z、W、T,它们的原子序数依次增大.X是空气中含量最多的元素;Y、W位于同周期,W单质在常温下是黄绿色气体,Y单质在其中燃烧发出黄色火焰;Z的氧化物常用作制备通讯光纤;T是常见金属,在氧气中燃烧可以得到具有磁性的黑色物质.回答下列问题:
已知前四周期五种元素X、Y、Z、W、T,它们的原子序数依次增大.X是空气中含量最多的元素;Y、W位于同周期,W单质在常温下是黄绿色气体,Y单质在其中燃烧发出黄色火焰;Z的氧化物常用作制备通讯光纤;T是常见金属,在氧气中燃烧可以得到具有磁性的黑色物质.回答下列问题: