题目内容
已知A元素原子核外电子共占有5个轨道且有2个成单电子;B元素原子核外能量最高电子为:n=3、l=1、m=1、ms=+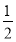 ,n=3、l=1、m=0、ms=+
,n=3、l=1、m=0、ms=+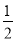 。则A、B两元素所形成化合物的晶体类型为( )。
。则A、B两元素所形成化合物的晶体类型为( )。
A.分子晶体 B.原子晶体 C.离子晶体 D.金属晶体
B
【解析】A的核外电子排布式为1s22s22p4,A为O元素;B有3个电子层,且最高能量的电子有2个且为p电子,那么B为1s22s22p63s23p2,B为Si。SiO2为原子晶体。

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目
一定温度下,在2 L密闭容器中发生下列反应:4NO2(g)+O2(g) 2N2O5(g);已知该反应的平衡常数:K300 ℃>K350 ℃,且n(NO2)(单位:mol)随时间变化如下表:
2N2O5(g);已知该反应的平衡常数:K300 ℃>K350 ℃,且n(NO2)(单位:mol)随时间变化如下表:
时间(s) | 0 | 500 | 1000 | 1500 |
t1℃ | 20 | 13.96 | 10.08 | 10.08 |
t2℃ | 20 | a | b | c |
下列说法一定正确的是( )
A.正反应为吸热反应
B.如果t2℃<t1℃,那么a>b=c,且a=10+0.5b
C.如果t2℃<t1℃,那么t2℃达到平衡的时间介于1 000 s至1 500 s之间
D.如果t2℃>t1℃,那么b>10.08
下列数据对应物质的熔点,据此作出下列判断中错误的是( )。
Na2O | NaCl | AlF3 | AlCl3 |
920 ℃ | 801 ℃ | 1 292 ℃ | 190 ℃ |
BCl3 | Al2O3 | CO2 | SiO2 |
-107 ℃ | 2 073 ℃ | -57 ℃ | 1 723 ℃ |
A.铝的化合物的晶体中有离子晶体
B.表中只有BCl3和干冰是分子晶体
C.同族元素的氧化物可形成不同类型的晶体
D.不同族元素的氧化物可形成相同类型的晶体