题目内容
【题目】对于可逆反应:2A(g)+B(g)2C(g)△H<0,下列各图中正确的是( )
A.
B.
C.
D.
【答案】A
【解析】解:A、该反应为放热反应,温度升高平衡向逆反应方向移动,C的质量分数减小,故A正确;
B、根据反应前后的化学计量数的大小可以看出,增大压强平衡向正反应方向移动,正逆反应速率都增大,且V正>V逆 , 故B错误;
C、催化剂同等程度地改变正逆反应速率,平衡不发生移动,故C错误;
D、该反应为放热反应,温度升高平衡向逆反应方向移动,A的转化率降低,根据反应前后的化学计量数的大小可以看出,增大压强平衡向正反应方向移动,A的转化率增大,本题温度的曲线不正确,故D错误.
故选A.
做题时首先分析化学方程式的特征,如反应前后计量数的大小关系、反应热等问题,
A、根据反应温度的不同结合反应热判断平衡移动的方向,可判断出C的质量分数的变化是否正确
B、根据反应前后的化学计量数的大小关系,结合压强对反应速率的影响判断平衡移动方向,从而判断出正逆反应速率的变化;
C、从催化剂对平衡是否有影响来判断浓度的变化是否正确;
D、从两个方面考虑,一是压强对平衡的影响,二是温度对平衡的影响,二者结合判断A的转化率是否正确.

【题目】氮的固定一直是科学家研究的重要课题,合成氨则是人工固氮比较成熟的技术,其原理为N2 (g)+3H2 (g)2NH3(g)△H.
(1)已知每破坏1mol有关化学键需要的能量如表:
H﹣H | N﹣H | N﹣N | N |
435.9KJ | 390.8KJ | 192.8KJ | 945.8KJ |
则△H= .
(2)在恒温、恒压容器中,氨体积比1:3加入N2和H2进行合成氨反应,达到平衡后,再向容器中充入适量氨气,达到新平衡时,c(H2)将(填“增大”“减小”或“不变”)
(3)在不同温度、压强和相同催化剂条件下,初始时N2、H2分别为0.1mol、0.3mol时,平衡后混合物中氨的体积分数(φ)如图所示. 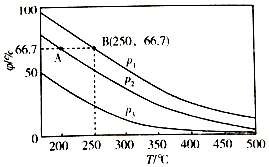
①其中,p1、p2和p3由大到小的顺序是 , 其原因是 .
②若分别用vA(N2)和vB(N2)表示从反应开始至达平衡状态A、B时的化学反应速率,则vA(N2)vB(N2)(填“>”“<”或“=”)
③若在250℃、p1条件下,反应达到平衡时容器的体积为1L,则该条件下合成氨的平衡常数K=(保留一位小数).
(4)H2NCOONH4是工业由氨气合成尿素的中间产物.在一定温度下、体积不变的密闭容器中发生反应:H2NCOONH4(s)2NH3(g)+CO2(g),能说明该反应达到平衡状态的是(填序号). ①混合气体的压强不变
②混合气体的密度不变
③混合气体的总物质的量不变
④混合气体的平均相对分子质量不变
⑤NH3的体积分数不变.
【题目】在300mL的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:Ni(s)+4CO(g)Ni(CO)4(g),已知该反应平衡常数与温度的关系如表:
温度/℃ | 25 | 80 | 230 |
平衡常数 | 5×104 | 2 | 1.9×10﹣5 |
下列说法不正确的是( )
A.上述生成Ni(CO)4(g)的反应为放热反应
B.25℃时反应Ni(CO)4(g)Ni(s)+4CO(g)的平衡常数为2×10﹣5
C.80℃达到平衡时,测得n(CO)=0.3mol,则Ni(CO)4的平衡浓度为2 mol/L
D.在80℃时,测得某时刻,Ni(CO)4、CO浓度均为0.5 mol/L,则此时v(正)>v(逆)