题目内容
8.有关碳元素及其化合物的化学用语正确的是( )| A. | CO2的电子式: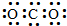 | B. | 乙烯的比例模型: | ||
| C. | 醋酸钠的分子式:C2H3O2Na | D. | C原子最外层电子的轨道表示式: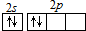 |
分析 A.二氧化碳分子中存在两个碳氧双键,碳原子最外层达到8电子稳定结构;
B.乙烯分子中存在碳碳双键,为平面结构,碳原子相对体积大于氢原子;
C.醋酸钠为离子化合物,不存在醋酸钠分子;
D.原子轨道表示式遵循洪特规则,电子尽可能分占单独轨道.
解答 解:A.二氧化碳为共价化合物,分子中存在碳氧双键,二氧化碳正确的电子式为: ,故A错误;
,故A错误;
B.C原子比H原子大,黑色球表示C原子,且乙烯为平面结构,则乙烯的比例模型为 ,故B正确;
,故B正确;
C.醋酸钠为离子晶体,不存在分子式,只能说是化学式,故C错误;
D.2p电子应该单独占有1个轨道,C原子最外层电子的轨道表示式为: ,故D错误;
,故D错误;
故选B.
点评 本题考查考查了常见化学用语的表示方法,题目难度中等,涉及电子轨道排布式、电子式、比例模型、化学式与分子式等知识,明确常见化学用语的概念及书写原则为解答关键.

练习册系列答案
相关题目
18.下列说法正确的是( )
| A. | 用pH试纸测氯水的pH | |
| B. | 用磨口玻璃瓶保存NaOH溶液 | |
| C. | 中和滴定时锥形瓶使用前需用待测液润洗 | |
| D. | 用CS2可除去试管内壁残留的S |
19.常温下,下列各溶液的叙述正确的是( )
| A. | pH=7的NaHSO3与Na2SO3混合溶液中:c(Na+)=c(HSO3-)+c(SO32-) | |
| B. | 等物质的量浓度的下列溶液中:①NH4Al(SO4)2 ②NH4Cl ③CH3COONH4④NH3•H2O,c(NH4+)由大到小的顺序是①>②>③>④ | |
| C. | 0.1 mol•L-1的醋酸的pH=a,0.01 mol•L-1的醋酸的pH=b,则a+1=b | |
| D. | 0.1 mol•L-1的醋酸钠溶液20 mL与0.1 mol•L-1的盐酸10 mL混合后溶液显酸性,则有:c(CH3COOH)>c(Cl-)>c(CH3COO-)>c(H+)>c(OH-) |
16.1869年,俄国化学家门捷列夫制作出了第一张元素周期表,揭示了化学元素间的内在联系,成为化学发展史上的重要里程碑之一,下列有关我们常用的元素周期表的说法正确的是( )
| A. | ⅠA族的元素全部都是金属元素 | |
| B. | 元素周期表与18个纵行,即有18个族 | |
| C. | 同周期中的IA族元素的金属性比ⅡA族元素的金属性强 | |
| D. | 元素周期表中右上方区域的元素多用于制造半导体材料 |
3.下列反应的离子方程式正确的是( )
| A. | 向NaOH溶液中通入过量的CO2气体:CO2+2OH-═HCO3-+H2O | |
| B. | 过量氢氧化钙与碳酸氢镁溶液反应:HCO3-+Ca2++OH-═CaCO3↓+H2O | |
| C. | Fe3O4与稀硝酸反应:Fe2O3+8H+═Fe2++Fe3++4H2O | |
| D. | 偏铝酸钠溶液中加入过量盐酸:AlO2-+4H+═Al3++2H2O |
20.下列物质显示酸性,且能发生酯化反应和消去反应的是( )
| A. | 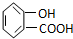 | B. | CH3CH2=CHCOOH | C. | 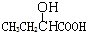 | D. | 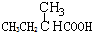 |
17.化学用语是学习化学的重要工具,下列化学用语中正确的是( )
| A. | Na2S的水解:S2-+2H2O?H2S+2OH- | |
| B. | NaHCO3的电离:NaHCO3 ?Na++H++CO32- | |
| C. | HSO3-的电离:HSO3-?H++SO32- | |
| D. | 钢铁的电化学腐蚀的负极反应式:Fe-3e-═Fe3+ |
18.有机物丁香油酚结构简式为: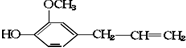 其可能具有的性质是:①能发生加成反应,②能使酸性高锰酸钾溶液褪色,③能发生取代反应,④能与三氯化铁发生显色反应,⑤能发生中和反应,⑥能发生消去反应( )
其可能具有的性质是:①能发生加成反应,②能使酸性高锰酸钾溶液褪色,③能发生取代反应,④能与三氯化铁发生显色反应,⑤能发生中和反应,⑥能发生消去反应( )
 其可能具有的性质是:①能发生加成反应,②能使酸性高锰酸钾溶液褪色,③能发生取代反应,④能与三氯化铁发生显色反应,⑤能发生中和反应,⑥能发生消去反应( )
其可能具有的性质是:①能发生加成反应,②能使酸性高锰酸钾溶液褪色,③能发生取代反应,④能与三氯化铁发生显色反应,⑤能发生中和反应,⑥能发生消去反应( )| A. | 全部 | B. | 仅①②③④ | C. | 除⑥外都能 | D. | 除④⑥外都能 |
 原子序数小于36的X、Y、Z、W四种元素,其中X是形成化合物种类最多的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W的原子序数为29.回答下列问题:
原子序数小于36的X、Y、Z、W四种元素,其中X是形成化合物种类最多的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W的原子序数为29.回答下列问题: