题目内容
在锌跟稀硝酸反应时,若参加反应的锌与消耗的硝酸的物质的量之比为1:2.5时,则被还原的HNO3和未被还原的HNO3的物质的量之比为
| A.2:5 | B.1:4 | C.1:5 | D.1:9 |
BD
Zn与HNO3的物质的量比为1:2.5即4:10。
则:4Zn+10HNO3="4Zn" (NO3)2+N2O↑+5H2O ……………………①
4Zn+10HNO3="4Zn" (NO3)2+NH4NO3↑+3H2O ……………………②
按反应①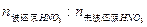 =1:4,按反应②
=1:4,按反应②
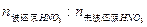 =1:9
=1:9
则:4Zn+10HNO3="4Zn" (NO3)2+N2O↑+5H2O ……………………①
4Zn+10HNO3="4Zn" (NO3)2+NH4NO3↑+3H2O ……………………②
按反应①
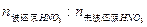 =1:4,按反应②
=1:4,按反应②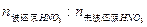 =1:9
=1:9
练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目