题目内容
a mol氨完全氧化成HNO3,并且全部溶于反应生成的水中,得HNO3的质量分数约为
| A.78% | B.42% | C.50% | D.63% |
A
NH3+2O2===HNO3+H2O?
HNO3%=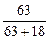 ×100%=78%
×100%=78%
HNO3%=
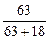 ×100%=78%
×100%=78%
练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
题目内容
| A.78% | B.42% | C.50% | D.63% |
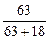 ×100%=78%
×100%=78%
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案