题目内容
(1)标准状况下,①4g氢气、②33.6L甲烷(CH4)、③6.02×1023个水分子中,物质的量最大的是(填写序号,下同)______,体积最大的是______.
(2)质量相等的两种物质SO2和SO3,它们的物质的量之比为______,所含氧原子个数之比为______.
解:(1)①氢气的物质的量为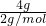 =2mol,②标准状况下甲烷的物质的量为
=2mol,②标准状况下甲烷的物质的量为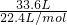 =1.5mol,③水的物质的量为
=1.5mol,③水的物质的量为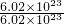 =1mol,
=1mol,
显然物质的量最大的是①,相同状况下,物质的量越大,气体的体积越大,则体积最大的为①,故答案为:①;①;
(2)设二者的质量均为64g,则SO2的物质的量为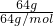 =1mol,SO3的物质的量为
=1mol,SO3的物质的量为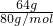 =0.8mol,
=0.8mol,
则它们的物质的量之比为1mol:0.8mol=5:4,所含氧原子个数之比为1mol×2:0.8mol×3=5:6,故答案为:5:4;5:6.
分析:(1)利用n= =
=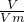 =
= 来计算物质的量,物质的量最大的则体积最大;
来计算物质的量,物质的量最大的则体积最大;
(2)利用n= 及物质的构成来分析所含氧原子个数之比.
及物质的构成来分析所含氧原子个数之比.
点评:本题考查有关物质的量的计算,明确以物质的量为中心的基本计算公式即可解答,(2)中巧设物质的质量是关键.
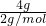 =2mol,②标准状况下甲烷的物质的量为
=2mol,②标准状况下甲烷的物质的量为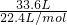 =1.5mol,③水的物质的量为
=1.5mol,③水的物质的量为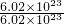 =1mol,
=1mol,显然物质的量最大的是①,相同状况下,物质的量越大,气体的体积越大,则体积最大的为①,故答案为:①;①;
(2)设二者的质量均为64g,则SO2的物质的量为
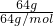 =1mol,SO3的物质的量为
=1mol,SO3的物质的量为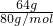 =0.8mol,
=0.8mol,则它们的物质的量之比为1mol:0.8mol=5:4,所含氧原子个数之比为1mol×2:0.8mol×3=5:6,故答案为:5:4;5:6.
分析:(1)利用n=
 =
=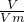 =
= 来计算物质的量,物质的量最大的则体积最大;
来计算物质的量,物质的量最大的则体积最大;(2)利用n=
 及物质的构成来分析所含氧原子个数之比.
及物质的构成来分析所含氧原子个数之比.点评:本题考查有关物质的量的计算,明确以物质的量为中心的基本计算公式即可解答,(2)中巧设物质的质量是关键.

练习册系列答案
相关题目
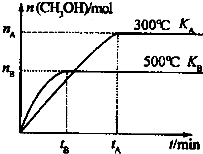 CO和H2与我们的生产和生活等方面密切相关.
CO和H2与我们的生产和生活等方面密切相关.