题目内容
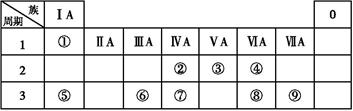
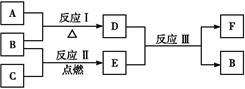
(10分)短周期元素A、B、C、D、E原子序数依次增大,A与C可形成A2C2和A2C两种化合物;B的最高价氧化物对应的水化物甲与其气态氢化物乙反应可生成盐丙;D与A位于同一主族;在同周期元素形成的简单离子中,E的离子半径最小。
(1)实验室中可用A2C2制取C单质,其化学方程式是
(2)由A、C、D三种元素组成的化合物的电子式是 ;B、C、E三种元素组成的常见盐的水溶液呈酸性,原因是 (用离子方程式表示)。
(3)反应乙+C2→B2+A2C(未配平)可设计为燃料电池,则通入乙的电极是 (填“正”或“负”)极,在碱性条件下其电极反应是
(1)实验室中可用A2C2制取C单质,其化学方程式是
(2)由A、C、D三种元素组成的化合物的电子式是 ;B、C、E三种元素组成的常见盐的水溶液呈酸性,原因是 (用离子方程式表示)。
(3)反应乙+C2→B2+A2C(未配平)可设计为燃料电池,则通入乙的电极是 (填“正”或“负”)极,在碱性条件下其电极反应是
(1)2H2O2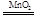 2H2O+O2↑;(2)
2H2O+O2↑;(2) ; NH4+ + H2O
; NH4+ + H2O  NH3·H2O + H+;
NH3·H2O + H+;
(3)负极, 2NH3+6OH-—6e- N2+6H2O。
N2+6H2O。
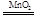 2H2O+O2↑;(2)
2H2O+O2↑;(2) ; NH4+ + H2O
; NH4+ + H2O  NH3·H2O + H+;
NH3·H2O + H+;(3)负极, 2NH3+6OH-—6e-
 N2+6H2O。
N2+6H2O。试题分析:根据题意知,短周期元素A、B、C、D、E原子序数依次增大,A与C可形成A2C2和A2C两种化合物,实验室中可用A2C2制取C单质,则A为氢元素,C为氧元素,A2C2为H2O2,A2C为H2O;B的最高价氧化物对应的水化物甲与其气态氢化物乙反应可生成盐丙,则B为氮元素,甲为硝酸,乙为氨气,丙为硝酸铵;D与A位于同一主族,则D为钠元素;在同周期元素形成的简单离子中,E的离子半径最小,则E为铝元素。(1)实验室中可用H2O2制取O2,其化学方程式是2H2O2
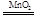 2H2O+O2↑;(2)由A、C、D三种元素组成的化合物氢氧化钠的电子式是
2H2O+O2↑;(2)由A、C、D三种元素组成的化合物氢氧化钠的电子式是 ;B、C、E三种元素组成的常见盐硝酸铵的水溶液呈酸性,原因是NH4+ + H2O
;B、C、E三种元素组成的常见盐硝酸铵的水溶液呈酸性,原因是NH4+ + H2O  NH3·H2O + H+;(3)反应NH3+O2→N2+H2O(未配平)可设计为燃料电池,氨气发生氧化反应,则通入氨气的电极是负极,在碱性条件下其电极反应是2NH3+6OH-—6e-
NH3·H2O + H+;(3)反应NH3+O2→N2+H2O(未配平)可设计为燃料电池,氨气发生氧化反应,则通入氨气的电极是负极,在碱性条件下其电极反应是2NH3+6OH-—6e- N2+6H2O。
N2+6H2O。
练习册系列答案
相关题目