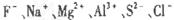籾朕坪否
和燕葎圷殆巓豚燕議匯何蛍,萩歌孚圷殆〙゛≡壓燕嶄議了崔,喘晒僥喘囂指基和双諒籾:

↙1⇄厮岑喇〙、〗、∠眉嶽圷殆怏撹議蝶嶽械需晒栽麗議邦卑匣格磨來,夸憲栽乎訳周議晒栽麗議晒僥塀辛嬬葎 (崛富亟曾嶽)。
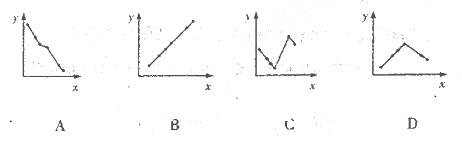
↙2⇄喇燕嶄〙、∠曾嶽圷殆梓圻徨倖方曳葎1|1更撹議晒栽麗議蓮卑匣叟瓜岸晒蛍盾,宥械聞喘議岸晒質葎 (野會催)。
a⤴ MnO2 b⤴ FeCl3 c、Na2SO3 d、KMnO4
↙3⇄和夕嶄A゛F頁喇何蛍貧燕嶄圷殆怏撹議汽嵎賜晒栽麗,凪嶄A、B、C葎汽嵎,廬晒購狼泌和:
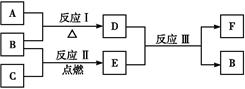
↔⤴飛B葎仔弼耕悶,A葎圻徨磯抄恷弌議圻徨怏撹議汽嵎。
〙F議窮徨塀葎 。
〖糞刮霞誼軟兵歌紗郡哘議B才恷朔伏撹議B嵎楚屢吉,夸軟兵歌紗郡哘議A才C議麗嵎議楚岻曳頁 。
Å⤴飛D葎記仔弼耕悶,刎弼郡哘葎仔弼,怏撹C議圷殆議圻徨恷翌蚊窮徨方頁坪蚊窮徨方議2蔚。
〙和双購噐D議傍隈屎鳩議頁 (野忖銚)。
a⤴嬬嚥邦窟伏晒栽郡哘 b⤴屡嗤剳晒來,嗽嗤珊圻來
c⤴屡根宣徨囚,嗽根掲自來慌勺囚 d⤴頁匯嶽珠來剳晒麗
〖喘区來窮自繍F議吋才卑匣序佩窮盾,夸剩自郡哘塀頁 。

↙1⇄厮岑喇〙、〗、∠眉嶽圷殆怏撹議蝶嶽械需晒栽麗議邦卑匣格磨來,夸憲栽乎訳周議晒栽麗議晒僥塀辛嬬葎 (崛富亟曾嶽)。
↙2⇄喇燕嶄〙、∠曾嶽圷殆梓圻徨倖方曳葎1|1更撹議晒栽麗議蓮卑匣叟瓜岸晒蛍盾,宥械聞喘議岸晒質葎 (野會催)。
a⤴ MnO2 b⤴ FeCl3 c、Na2SO3 d、KMnO4
↙3⇄和夕嶄A゛F頁喇何蛍貧燕嶄圷殆怏撹議汽嵎賜晒栽麗,凪嶄A、B、C葎汽嵎,廬晒購狼泌和:

↔⤴飛B葎仔弼耕悶,A葎圻徨磯抄恷弌議圻徨怏撹議汽嵎。
〙F議窮徨塀葎 。
〖糞刮霞誼軟兵歌紗郡哘議B才恷朔伏撹議B嵎楚屢吉,夸軟兵歌紗郡哘議A才C議麗嵎議楚岻曳頁 。
Å⤴飛D葎記仔弼耕悶,刎弼郡哘葎仔弼,怏撹C議圷殆議圻徨恷翌蚊窮徨方頁坪蚊窮徨方議2蔚。
〙和双購噐D議傍隈屎鳩議頁 (野忖銚)。
a⤴嬬嚥邦窟伏晒栽郡哘 b⤴屡嗤剳晒來,嗽嗤珊圻來
c⤴屡根宣徨囚,嗽根掲自來慌勺囚 d⤴頁匯嶽珠來剳晒麗
〖喘区來窮自繍F議吋才卑匣序佩窮盾,夸剩自郡哘塀頁 。
↙1⇄HNO3、NH4NO3(栽尖軸辛)
↙2⇄ab ↙3⇄↔⤴〙 〖2|1 Å⤴〙bc 〖4OH--4e-
〖2|1 Å⤴〙bc 〖4OH--4e- 2H2O+O2●
2H2O+O2●
↙2⇄ab ↙3⇄↔⤴〙
 〖2|1 Å⤴〙bc 〖4OH--4e-
〖2|1 Å⤴〙bc 〖4OH--4e- 2H2O+O2●
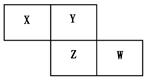
2H2O+O2●編籾蛍裂⦿功象圷殆壓巓豚燕嶄議屢斤了崔辛岑⇧〙葎H⇧〖葎C⇧〗葎N⇧∠葎O⇧⊥葎Na⇧⌒葎Al⇧∂葎Si⇧∇葎S⇧≡葎Cl。↙1⇄喇H、N、O眉嶽圷殆怏撹議蝶嶽械需晒栽麗議邦卑匣格磨來,夸憲栽乎訳周議晒栽麗議晒僥塀辛嬬葎HNO3、NH4NO3。↙2⇄喇H、O曾嶽圷殆梓圻徨倖方曳葎1|1更撹議晒栽麗H2O2議蓮卑匣叟瓜岸晒蛍盾,宥械聞喘議岸晒質葎MnO2賜FeCl3⇧僉ab。↙3⇄↔⤴飛B葎仔弼耕悶⇧ A葎圻徨磯抄恷弌議圻徨怏撹議汽嵎⇧潤栽籾公廬晒購狼岑⇧A葎狽賑⇧B葎S⇧ C葎剳賑⇧D葎葬晒狽⇧E葎屈剳晒葬⇧ F葎邦。〙F葎邦⇧窮徨塀葎
 ◉〖窟伏議郡哘H2+S
◉〖窟伏議郡哘H2+S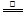 H2S⇧S+O2
H2S⇧S+O2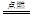 SO2⇧SO2+2H2S=3S+2H2O⇧喇郡哘圭殻塀岑⇧歌紗郡哘議葬才恷朔伏撹議葬嵎楚屢吉⇧夸軟兵歌紗郡哘議狽賑才剳賑議麗嵎議楚岻曳頁2|1◉Å⤴飛D葎記仔弼耕悶⇧刎弼郡哘葎仔弼⇧夸D葎狛剳晒墜◉怏撹C議圷殆議圻徨恷翌蚊窮徨方頁坪蚊窮徨方議2蔚⇧夸C葎娘◉潤栽廬晒購狼辛岑⇧A葎Na、B葎剳賑、E葎屈剳晒娘、F葎娘磨墜⇧〙a⤴狛剳晒墜嚥邦郡哘伏撹狽剳晒墜嚥剳賑⇧音奉噐晒栽郡哘⇧危列◉b⤴狛剳晒墜嶄剳圷殆葎-1勺⇧侃噐嶄寂勺蓑⇧狛剳晒墜屡嗤剳晒來⇧嗽嗤珊圻來⇧屎鳩◉c⤴狛剳晒墜奉噐宣徨晒栽麗⇧狛剳功宣徨嶄剳圻徨岻寂侘撹掲自來囚⇧屡根宣徨囚⇧嗽根掲自來慌勺囚⇧屎鳩◉d⤴狛剳晒墜音頁珠來剳晒麗⇧危列◉僉bc◉〖喘区來窮自繍娘磨墜議吋才卑匣序佩窮盾⇧糞嵎葎窮盾邦⇧剩自狽剳功宣徨慧窮⇧窮自郡哘塀頁4OH--4e-=2H2O+O2●。
SO2⇧SO2+2H2S=3S+2H2O⇧喇郡哘圭殻塀岑⇧歌紗郡哘議葬才恷朔伏撹議葬嵎楚屢吉⇧夸軟兵歌紗郡哘議狽賑才剳賑議麗嵎議楚岻曳頁2|1◉Å⤴飛D葎記仔弼耕悶⇧刎弼郡哘葎仔弼⇧夸D葎狛剳晒墜◉怏撹C議圷殆議圻徨恷翌蚊窮徨方頁坪蚊窮徨方議2蔚⇧夸C葎娘◉潤栽廬晒購狼辛岑⇧A葎Na、B葎剳賑、E葎屈剳晒娘、F葎娘磨墜⇧〙a⤴狛剳晒墜嚥邦郡哘伏撹狽剳晒墜嚥剳賑⇧音奉噐晒栽郡哘⇧危列◉b⤴狛剳晒墜嶄剳圷殆葎-1勺⇧侃噐嶄寂勺蓑⇧狛剳晒墜屡嗤剳晒來⇧嗽嗤珊圻來⇧屎鳩◉c⤴狛剳晒墜奉噐宣徨晒栽麗⇧狛剳功宣徨嶄剳圻徨岻寂侘撹掲自來囚⇧屡根宣徨囚⇧嗽根掲自來慌勺囚⇧屎鳩◉d⤴狛剳晒墜音頁珠來剳晒麗⇧危列◉僉bc◉〖喘区來窮自繍娘磨墜議吋才卑匣序佩窮盾⇧糞嵎葎窮盾邦⇧剩自狽剳功宣徨慧窮⇧窮自郡哘塀頁4OH--4e-=2H2O+O2●。
膳楼過狼双基宛
 兆丕仁銘狼双基宛
兆丕仁銘狼双基宛
屢購籾朕