题目内容
【题目】某校化学兴趣小组拟探究碳、硅元素的非金属性的相对强弱,实验装置如下:
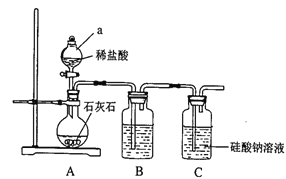
(1)连接好装置后,实验前必须进行的一步操作是_________。仪器a的名称为______。
(2)B装置中盛放的试剂是_________,C中发生反应的化学方程式为_________。
(3)该兴趣小组设计此实验依据的原理是_________,通过_________(填实验现象),可判断碳的非金属性强于硅的非金属性。请你再列举出一条事实,说明碳的非金{属性强于硅的非金属性:________。
(4)该小组的一位同学认为,利用此实验装置及药品,也可以证明非金属性Cl>C>Si,你是否同意该同学的观点?_________(填“同意”或“不同意”)。
【答案】 检查装置的气密性 分液漏斗 饱和NaHCO3溶液 Na2SiO3+CO2+H2O=Na2CO3+H2SiO3↓ 元素的最高价氧化物对应的水化物酸性越强,元素的非金属性越强 C中有白色胶状沉淀生成 CH4比SiH4稳定或碳单质与氢气化合比硅单质与氢气化合容易(或其他合理答案,答碳单质置换出硅单质不给分) 不同意
【解析】(1)反应生成气体,实验之前需要检验装置的气密性,防止气密性不好导致气体泄漏。根据装置图中的仪器可知a为分液漏斗;(2)生成的CO2中含有氯化氢,氯化氢也能与硅酸钠反应,因此B装置中盛放的试剂是饱和碳酸氢钠溶液,用来除去氯化氢。C中发生CO2与硅酸钠的反应,反应的化学方程式为Na2SiO3+CO2+H2O=Na2CO3+H2SiO3↓;(3)二氧化碳与Na2SiO3溶液反应生成硅酸,证明了碳酸酸性比硅酸强,说明碳元素的非金属性比硅元素非金属性强,所以盛有Na2SiO3溶液的试管中出现白色沉淀即说明碳元素的非金属性比硅元素非金属性强;比较元素非金属性强弱,还可以通过氢化物稳定性或与氢气化合的难易程度等,即CH4比SiH4稳定或碳单质与氢气化合比硅单质与氢气化合容易均可以说明碳元素非金属性强于硅。(4)盐酸不是最高价含氧酸,因此不能证明非金属性Cl>C>Si。