题目内容
13.现有含NaCl、Na2SO4 和NaNO3 的混合溶液,选择适当的试剂将其转化为相应的沉淀或固体,从而实现Cl- 和NO3- 的相互分离.相应的实验过程如下: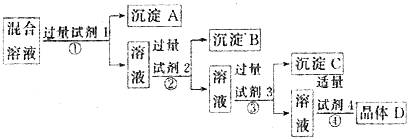
下列关于四种试剂顺序正确的是( )
| A. | 氯化钡溶液、硝酸银溶液、碳酸钠溶液、硝酸溶液 | |
| B. | 硝酸银溶液、氯化钡溶液、碳酸钠溶液、硝酸溶液 | |
| C. | 氯化钡溶液、硝酸银溶液、硝酸溶液、碳酸钠溶液 | |
| D. | 硝酸银溶液、碳酸钠溶液、氯化钡溶液、硝酸溶液 |
分析 如先加入AgNO3,则会同时生成Ag2SO4和AgCl沉淀,则应先加入过量的BaCl2[或Ba(NO3)2],生成BaSO4沉淀,然后在滤液中加入过量的AgNO3,使Cl-全部转化为AgCl沉淀,在所得滤液中加入过量的Na2CO3,使溶液中的Ag+、Ba2+完全沉淀,最后所得溶液为NaNO3和Na2CO3的混合物,加入稀HNO3,最后进行蒸发操作可得固体NaNO3.
解答 解:分离溶液中的Cl-,应加入AgNO3,分离溶液中的SO42-,应加入BaCl2[或Ba(NO3)2],如先加入AgNO3,则会同时生成Ag2SO4和AgCl沉淀,则应先加入过量的BaCl2
[或Ba(NO3)2],生成BaSO4沉淀,然后在滤液中加入过量的AgNO3,使Cl-全部转化为AgCl沉淀,在所得滤液中加入过量的Na2CO3,使溶液中的Ag+、Ba2+完全沉淀,最后所得溶液为NaNO3和Na2CO3的混合物,加入稀HNO3,最后进行蒸发操作可得固体NaNO3,所以试剂1为BaCl2[或Ba(NO3)2],试剂2为AgNO3,试剂3为Na2CO3,试剂4为HNO3,故选A.
点评 本题考查物质的分离提纯操作,题目难度中等,本题注意Cl-、SO42-的性质,把握除杂原则,提纯时不能引入新的杂质,注意把握实验的先后顺序.

练习册系列答案
相关题目
3.下列溶液中,粒子的物质的量浓度关系正确的是( )
| A. | 0.1mol•L-1Na2SO3溶液中:c(OH-)=c(HSO3-)+c(H+)+c(H2SO3) | |
| B. | 1L0.1mol•L-1CuCl2溶液中:c(Cl-)=2c(Cu2+) | |
| C. | 物质的量浓度相等的Na2S和NaHS的混合溶液中:2c(Na+)=3c(S2-)+3c(HS-)+3c(H2S) | |
| D. | 室温时,向一定物质的量浓度的CH3COOH溶液中加入一定体积的氢氧化钠溶液,充分反应后溶液的pH=7,则反应后的溶液中:c(CH3COO-)>c(Na+)>c(H+)=c(OH-) |
4.下列变化中不需要破坏化学键的是( )
| A. | 氯化钠熔化 | B. | 干冰气化 | C. | 金刚石熔化 | D. | 氯化氢溶于水 |
1.下列变化过程中,原物质分子内共价键被破坏,同时有离子键形成的是( )
| A. | 盐酸和NaOH溶液混合 | B. | 氯化氢溶于水 | ||
| C. | 溴化氢气体与氨气相遇反应 | D. | 锌和稀硫酸反应 |
5.NA代表阿伏加德罗常数,下列有关叙述正确的是( )
| A. | 1mol苯分子中含有碳碳双键数为3NA | |
| B. | 1mol氯化氢分子中含H+离子数为NA | |
| C. | 16 gCH4与18g NH4+ 所含质子数均为NA | |
| D. | 4.6 g钠与足量盐酸完全反应失去电子数为0.2NA |
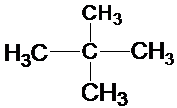 和
和 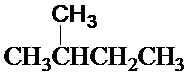
 A、B、C、D、E、F分别是氧化铁、二氧化碳、稀盐酸、氢氧化钙溶液、碳酸钠溶液、氢氧化钠溶液中的一种;已知C在日常生活中常用来灭火.六种物质之间有如图所示的反应关系,图中相连的两圆表示相应物质间能发生反应.回答下列问题:
A、B、C、D、E、F分别是氧化铁、二氧化碳、稀盐酸、氢氧化钙溶液、碳酸钠溶液、氢氧化钠溶液中的一种;已知C在日常生活中常用来灭火.六种物质之间有如图所示的反应关系,图中相连的两圆表示相应物质间能发生反应.回答下列问题: