题目内容
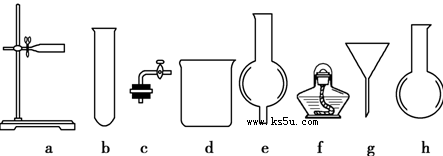
下列有关实验装置的说法,正确的是 
| A.用图1装置制取干燥纯净的NH3 |
| B.用图2装置制备Fe(OH)2并能较长时间观察其颜色 |
| C.用图3装置可以完成“喷泉”实验 |
| D.用图4装置测量Cu与浓硝酸反应产生气体的体积 |
C
解析试题分析:A.NaOH固体有吸水性,吸水放热,可以使氨水分解产生氨气和水。碱石灰是碱性干燥剂,可以干燥氨气等碱性气体,但是氨气的密度比空气小,不能用向上排空气法收集,应该用向下排空气法收集。错误。B.若要制备Fe(OH)2并能较长时间观察其颜色,应该使Fe与电源的正极相连,作阳极,电极反应为:Fe-2e-=Fe2+.产生的Fe2+与溶液中OH-发生离子反应:Fe2++2OH-=Fe(OH)2↓.错误。C. 挤压胶头滴管,这时NaOH溶液进入到烧瓶中,发生反应:2NaOH+Cl2=NaCl+NaClO,反应使容器内的气体压强减小,小于外界大气压强,烧杯内的NaOH溶液就会会不断的进入到烧瓶,因而就形成了喷泉实验。正确。D. Cu与浓硝酸反应的方程式为:Cu+4HNO3(浓)=Cu(NO3)2+NO2↑+2H2O,反应产生的NO2气体会与水发生反应:3NO2+ H2O = 2HNO3+ NO。因此就无法确定气体的体积了。错误。
考点:考查关于物质的制取、收集、干燥剂性质的知识。

练习册系列答案
相关题目
下列各组中的实验步骤及现象,能达到相应实验目的的是
| | 实验目的 | 实验步骤及现象 |
| A | 检验亚硫酸钠试样是否变质 | 试样  白色沉淀 白色沉淀 沉淀不溶解 沉淀不溶解 |
| B | 制取氯气并探究氯气是否具有漂白性 | MnO2和稀盐酸 气体 气体 褪色 褪色 |
| C | 证明酸性条件H2O2氧化性比I2强 | 碘化钠溶液  溶液变蓝色 溶液变蓝色 |
| D | 探究浓度对于化学平衡的影响 | FeCl3和KSCN混合溶液 红色变深 红色变深 |
某同学想用实验证明FeCl3溶液显黄色不是氯离子造成的,下列实验无意义的是
| A.观察KCl溶液没有颜色 |
| B.向FeCl3溶液中滴加适量NaOH溶液,振荡静置,过滤后所得滤液黄色消失 |
| C.向FeCl3溶液中滴加适量AgNO3溶液,振荡静置,过滤后所得滤液黄色未消失 |
| D.加水稀释后FeCl3溶液黄色变浅 |
某学生用质量为a g、边长为b cm的正方形镀锌铁片与过量盐酸反应测定镀层厚度,并将实验结果绘图示意,反应完毕后铁片质量为c g(已知锌的密度为ρ g/cm3)。下列叙述错误的是
| A.t1时刻锌镀层已完全反应 |
B.锌镀层的厚度为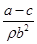 |
| C.反应放热也是影响OA段的反应速率的因素之一 |
| D.有原电池反应发生,正极的电极反应式为Zn - 2e → Zn2+ |
下列实验操作正确且能达到预期目的的是
| | 实验目的 | 操作 |
| A | 比较水和乙醇中羟基氢的活泼性强弱 | 用金属钠分别与水和乙醇反应 |
| B | 欲证明CH2=CHCHO中含有碳碳双键 | 滴入KMnO4酸性溶液,看紫红色是否褪去 |
| C | 确定磷、砷两元素非金属性的强弱 | 测定同温同浓度的Na3PO4和Na3AsO4水溶液的pH |
| D | 欲除去苯中混有的苯酚 | 向混合液中加入浓溴水,充分反应后,过滤 |
下列实验对应的结论不正确的是( )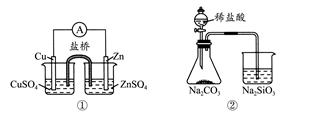
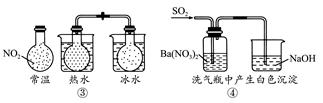
| A.①能组成Zn-Cu原电池 |
| B.②能证明非金属性Cl>C>Si |
C.③说明反应2NO2(g)  N2O4(g),ΔH<0 N2O4(g),ΔH<0 |
| D.④白色沉淀为BaSO4 |
下列关于各实验装置图的叙述中正确的是( )。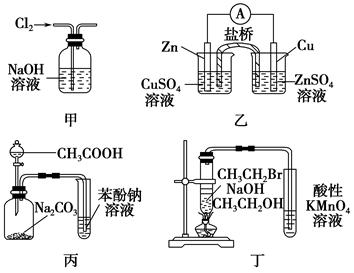
| A.图甲:除去Cl2中含有的少量HCl |
| B.图乙:构成锌—铜原电池 |
| C.图丙:根据实验现象推知酸性CH3COOH>H2CO3>C6H5OH |
| D.图丁:验证溴乙烷发生消去反应生成烯烃 |