题目内容
(8分)(1)将锌片和银片浸入稀硫酸中组成原电池,两电极间连接一个电流计。锌片上发生的电极反应: ;银片上发生的电极反应: 。
(2)若该电池中两电极的总质量为60g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为47g,试计算:产生氢气的体积(标准状况)。
(1)Zn-2e-=Zn2+;2H++2e-=H2↑
(2)4.48L
解析试题分析:(1)锌片、银片、稀硫酸构成原电池,锌作负极,负极上锌失电子发生氧化反应,电极反应式为:Zn-2e-=Zn2+;银作正极,正极上氢离子得电子发生还原反应,电极反应式为2H++2e-=H2↑。
(2)该原电池中,负极上锌失电子变成锌离子进入溶液,导致质量减少,正极上金属不参加反应,所以该装置中减少的质量是锌的质量,根据转移电子相等知,生成氢气的物质的量和锌的物质的量相等,所以生成气体的体积=(60—47)g÷65g/mol×22.4L/mol=4.48L。
考点:本题考查原电池原理及相关计算。

下图是氢氧燃料电池构造示意图。下列说法不正确的是
| A.a极是负极 |
| B.电子由b通过灯泡流向a |
| C.该电池总反应是2H2+ O2= 2H2O |
| D.该装置可将化学能转化为电能 |
电池是人类生产和生活中的重要能量来源,各式各样电池的发明是化学对人类的一项重大贡献。下列有关电池的叙述正确的是( )
| A.锌锰干电池工作一段时间后碳棒变细 |
| B.氢氧燃料电池可将热能直接转变为电能 |
| C.氢氧燃料电池工作时氢气在负极被氧化 |
| D.太阳能电池的主要材料是高纯度的二氧化硅 |
已知外电路中,电子由铜流向a极。有关下图所示的装置分析合理一项是( )
| A.该装置中Cu极为正极 |
| B.当铜极的质量变化为12.8 g时,a极上消耗的O2在标准状况下的体积为2.24 L |
C.b极反应的电极反应式为:H2一2 = 2H+ = 2H+ |
| D.一段时间后锌片质量减少 |
将纯锌片和纯铜片按图所示方式插入相同浓度的稀硫酸中,以下有关叙述中正确的是 
| A.甲装置中铜片表面有气泡生成 | B.乙装置中电能转化为化学能 |
| C.甲装置中电能转化为化学能 | D.乙装置中铜片表面有气泡生成 |
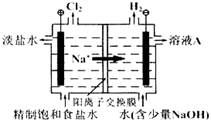
工业上电解制碱的技术是用阳离子交换膜法,主要原料是饱和食盐水。下图为阳离子交换膜法电解原理示意图:
请回答下列问题:
(1)A极为电解槽的________极,B极的材料工业上常采用的是生活中常见的金属,但有大量损耗,其主要原因是 。(填“吸氧腐蚀”或“析氢腐蚀”)
(2)电解槽中部的阳离子交换膜把电解槽隔成了阴极室和阳极室,这种阳离子交换膜,只允许溶液中的__________通过(填写下列微粒的编号)。
①H2,②Cl2,③H+,④Cl-,⑤Na+,⑥OH-。
(3)若上述电解过程中用阴离子交换膜代替阳离子交换膜(已知:3Cl2 +6OH-==5Cl-+ClO3-+3H2O),下列说法正确的组合是 。
| A.电解结束时,右侧溶液中含有ClO3— |
B.电解槽内发生反应的总化学方程式为:NaCl + 3H2O  NaClO3 + 3H2↑ NaClO3 + 3H2↑ |
| C.用阴离子交换膜后,电解槽内两个电极发生的电极反应与原来一样 |
| D.用阴离子交换膜后,阳离子的定向移动方向与原来相反 |