题目内容
【题目】相对分子质量为Mr的气态化合物V L(标准状况)溶于mg水中,得到溶液的质量分数为w%,物质的量浓度为cmol·L-1,密度为ρg·cm-3,则下列说法不正确的是( )
A.溶液密度ρ可表示为![]()
B.物质的量浓度c可表示为![]()
C.溶液的质量分数w%可表示为![]()
D.相对分子质量Mr可表示为![]()
【答案】C
【解析】
A.设溶液体积为xcm3,根据密度ρ=![]() 计算;
计算;
B.先根据m=nM计算出该气体得到质量,从而可知所得溶液质量,然后根据V=![]() 计算出溶液体积,最后根据c=
计算出溶液体积,最后根据c=![]() 计算出该溶液的浓度c;
计算出该溶液的浓度c;
C.根据溶质质量分数w%=![]() 计算;
计算;
D.先根据n=![]() 计算出该气体的物质的量,再结合水的质量、溶质质量分数计算出溶液中含有该气体质量,最后根据M=
计算出该气体的物质的量,再结合水的质量、溶质质量分数计算出溶液中含有该气体质量,最后根据M=![]() 计算出其摩尔质量。
计算出其摩尔质量。
A.设溶液体积为xcm3,该溶液中含有溶质的质量为:Mrg/mol×cmol/L×x×103L=cMx×103g,该溶液质量为:![]() ,该溶液的密度为:ρ=
,该溶液的密度为:ρ=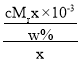 gcm3=
gcm3=![]() gcm3,故A正确;
gcm3,故A正确;
B.该气体的物质的量为![]() mol,该气体质量为:
mol,该气体质量为:![]() mol×Mrg/mol=
mol×Mrg/mol=![]() g,所得溶液质量为:mg+
g,所得溶液质量为:mg+![]() g,所得溶液的体积为:
g,所得溶液的体积为: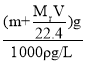 =
=![]() L,则该溶液的物质的量浓度为:c=
L,则该溶液的物质的量浓度为:c=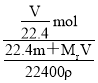 =
=![]() mol/L,故B正确;
mol/L,故B正确;
C.该气体质量为![]() g,所得溶液质量为(m+
g,所得溶液质量为(m+![]() )g,该溶液的质量分数为w%=
)g,该溶液的质量分数为w%=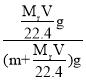 =
=![]() ,故C错误;
,故C错误;
D.标准状况下VL气体的物质的量为:![]() =
=![]() mol,水的质量分数为1w%,该溶液中含有该气体的质量为:
mol,水的质量分数为1w%,该溶液中含有该气体的质量为:![]() =
=![]() g,则该气体的摩尔质量为:M=
g,则该气体的摩尔质量为:M=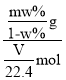 =
=![]() g/mol,该气体的相对分子质量为
g/mol,该气体的相对分子质量为![]() ,故D正确;
,故D正确;
故答案选C。

【题目】下列依据实验方案和现象对浓硫酸性质做出的判断合理的是
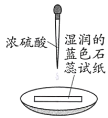
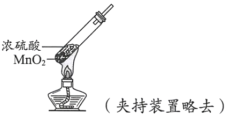
实验方案 | 实验I: | 实验II: |
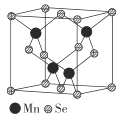
实验现象 | 试纸中心区域变黑,边缘变红 | 黑色固体溶解,溶液接近无色(溶液中锰元素仅以 |
A.由I可知,浓硫酸具有脱水性B.由I可知,浓硫酸具有弱酸性
C.由II可知,浓硫酸具有强氧化性D.由II可知,浓硫酸具有吸水性
【题目】二苯甲酮广泛应用于药物合成,同时也是有机颜料、杀虫剂等的重要中间体。实验室以苯与苯甲酰氯为原料,在AlCl3作用下制备二苯甲酮的实验流程如下图所示:

相关物理常数和物理性质如下表:
名称 | 相对分 子质量 | 密度/g·cm-3 | 熔点/oC | 沸点/oC | 溶解性 |
苯 | 78 | 0.88 | 5.5 | 80.1 | 难溶水,易溶乙醇 |
苯甲酰氯 | 140.5 | 1.22 | 1 | 197 | 遇水分解 |
无水氯化铝 | 133.5 | 2.44 | 190 | 178(升华) | 遇水水解,微溶苯 |
二苯甲酮 | 182 | 1.11 | 48.5 | 305(常压) | 难溶水,易溶苯 |
已知:反应原理为: 。该反应剧烈放热。
。该反应剧烈放热。
回答下列问题:
(1)反应装置如图所示(加热和夹持装置已略去),迅速称取7.5 g无水三氯化铝放入三颈瓶中,再加入30 mL无水苯,搅拌,缓慢滴加6 mL新蒸馏过的苯甲酰氯。反应液由无色变为黄色,三氯化铝逐渐溶解。混合完后,保持50℃左右反应1.5~2 h。
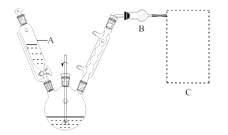
仪器A的名称为_______。装置B作用为_______。缓慢滴加苯甲酰氯的原因是______。能作为C中装置的是_______(填标号)。

(2)操作X为___________。
(3)NaOH溶液洗涤的目的是_____________。
(4)粗产品先经常压蒸馏除去__________,再减压蒸馏得到产品。
(5)当所测产品熔点为________时可确定产品为纯品。已知实验最终所得纯品8.0 g,则实验产率为_________ %(保留三位有效数字)。