题目内容
11.由CH4和O2组成的混合气体,标准状况下的密度为1g•L-1,则该混合气体中CH4和O2的质量比为( )| A. | 1:3 | B. | 1:2 | C. | 2:3 | D. | 3:4 |
分析 标准状况下的密度为1g•L-1,可知混合气体的相对分子质量为22.4,进而计算混合物的物质的量比和质量比.
解答 解:CH4和O2组成的混合气体,标准状况下的密度为1g•L-1,可知混合气体的相对分子质量为22.4,
设CH4和O2的物质的量分别为x、y,
则$\frac{16x+32y}{x+y}$=22.4,
x:y=3:2,
该混合气体中CH4和O2的质量比为3×16:2×32=3:4.
故选D.
点评 本题考查混合物的计算,为高频考点,侧重于学生的分析能力和计算能力的考查,难度不大.

练习册系列答案
相关题目
1.8.12天津港特大爆炸事故现场有700吨左右氰化钠,氰化钠剧毒.有少量因爆炸冲击发生泄漏.这些泄露的氰化钠可通过喷洒氧化剂双氧水的方式来处理,以减轻污染.
(1)写出NaCN的电子式Na+ ,偏碱性条件下,氰化钠溶液的CN-被双氧水氧化为HCO3-,同时放出NH3,该反应的离子方程式:CN-+H2O2+H2O═NH3↑+HCO3-.
,偏碱性条件下,氰化钠溶液的CN-被双氧水氧化为HCO3-,同时放出NH3,该反应的离子方程式:CN-+H2O2+H2O═NH3↑+HCO3-.
(2)Cu2+可作为双氧水氧化CN-中的催化剂.某兴趣小组要探究Cu2+对双氧水氧化CN-是否起催化作用,请你完成下实验方案.填写实验步骤、实验现象和结论(己知:CN-浓度可用离子色谱仪测定)
(1)写出NaCN的电子式Na+
 ,偏碱性条件下,氰化钠溶液的CN-被双氧水氧化为HCO3-,同时放出NH3,该反应的离子方程式:CN-+H2O2+H2O═NH3↑+HCO3-.
,偏碱性条件下,氰化钠溶液的CN-被双氧水氧化为HCO3-,同时放出NH3,该反应的离子方程式:CN-+H2O2+H2O═NH3↑+HCO3-.(2)Cu2+可作为双氧水氧化CN-中的催化剂.某兴趣小组要探究Cu2+对双氧水氧化CN-是否起催化作用,请你完成下实验方案.填写实验步骤、实验现象和结论(己知:CN-浓度可用离子色谱仪测定)
| 步骤:分别取等体积、等浓度的含氰废水于甲、乙两支试管中,再分别加入等体积、等浓度的双氧水溶液,只向甲试管中加入少量的无水硫酸铜粉末,用离子色谱仪测定相同反应时间内两支试管中的CN-浓度 | 现象与结论: 若若甲试管中的CN-浓度小于乙试管中的CN-浓度,则Cu2+对双氧水破氰反应起催化作用 若若两试管中的CN-浓度相同,则Cu2+对双氧水破氰反应不起催化作用 |
2.下列说法正确的是( )
| A. | 电池充电时其正极应与外电源的负极相连而成为阴极 | |
| B. | 氢氧燃料电池(碱性介质)的正极反应式:O2+4e-→2O2- | |
| C. | 粗铜精炼时,与电源正极相连的是纯铜 | |
| D. | 铁件上镀铜时,将铁件与电源的负极相连 |
19.下列物质中分子数最多的是( )
| A. | 标准状况下134.4LNH3 | B. | 132g CO2 | ||
| C. | 标准状况下108 mL 水 | D. | 6.02×1024个氢分子 |
6.实验室需用90mL0.1mol/L的硫酸铜溶液,用100mL的容量瓶配制,以下配制操作正确的是( )
| A. | 称取1.44g硫酸铜,配成100mL溶液 | B. | 称取2.25g胆矾,加入100mL水 | ||
| C. | 称取1.6g硫酸,加入100mL水 | D. | 称取2.5g胆矾,配成100mL溶液 |
16.用NA代表阿伏加德罗常数,下列表述正确的是( )
| A. | 1L0.5 mol•L-1CuCl2溶液中含有Cu2+的个数为0.5NA | |
| B. | 7.8g过氧化钠含有的共用电子对数为0.2NA | |
| C. | 25℃时,pH=13的1.0LBa(OH)2溶液中含有的OH-数目为0.1NA | |
| D. | 1mol羟基中电子数为10 NA |
3.标准状况下,现有①6.72L CH4 ②3.01×1023个HCl分子 ③13.6g H2S ④0.2mol NH3,对这四种气体的关系有以下四种表述,其中不正确的是( )
| A. | 体积:②>③>①>④ | B. | 物质的量:②>③>④>① | ||
| C. | 质量:②>③>①>④ | D. | 氢原子个数:①>③>④>② |
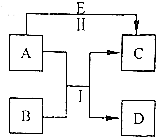 A、B、C、D、E是中学常见的五种物质,其转化关系如图所示,反应I、Ⅱ均在水溶液中进行,其中某些物质可能已略去.其中D是单质.C、E是化合物.若B是淡黄色粉末,反应I的原理用于呼吸面具中提供氧气.写出A的电子式
A、B、C、D、E是中学常见的五种物质,其转化关系如图所示,反应I、Ⅱ均在水溶液中进行,其中某些物质可能已略去.其中D是单质.C、E是化合物.若B是淡黄色粉末,反应I的原理用于呼吸面具中提供氧气.写出A的电子式 .
.