题目内容
在KI溶液中存在下列平衡:I2(aq)+I-(aq)=I(aq)。测得不同温度下该反应的平衡常数K如表所示,下列说法正确的是
A.反应I2(aq)+I-(aq) I(aq)的ΔH>0
I(aq)的ΔH>0
B.其他条件不变,升高温度,溶液中c(I)减小
C.该反应的平衡常数表达式为K=
D.25 ℃时,向溶液中加入少量KI固体,平衡常数K小于689
| t/℃ | 5 | 15 | 25 | 35 | 50 |
| K | 1 100 | 841 | 689 | 533 | 409 |
A.反应I2(aq)+I-(aq)
 I(aq)的ΔH>0
I(aq)的ΔH>0B.其他条件不变,升高温度,溶液中c(I)减小
C.该反应的平衡常数表达式为K=
D.25 ℃时,向溶液中加入少量KI固体,平衡常数K小于689
B
由题意知,温度升高,平衡常数减少,则平衡向逆方向移动,正反应为放热反应,A错;其他条件不变,升高温度,平衡向逆方向移动,溶液中c(I3-)减少,B正确;该反应的平衡常数表达式为K= c(I3-)/[ c(I-)c(I2)],C错;平衡常数只与温度有关,加放少量的KI固体对平衡没有影响,D错;答案选B。

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案
相关题目
 C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下: pC(气) + qD(气)的 C %与时间 t有如图关系
pC(气) + qD(气)的 C %与时间 t有如图关系
 NaCl(l)+ K(g)选适宜的温度,使K成蒸气从反应混合物中分离出来
NaCl(l)+ K(g)选适宜的温度,使K成蒸气从反应混合物中分离出来  MgO(s) + CO2(g) +SO2(g) △H>0该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是
MgO(s) + CO2(g) +SO2(g) △H>0该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是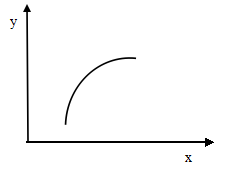
 2SO3(g)+Q (Q>0),将SO2转化为SO3,尾气SO2可用NaOH溶液进行吸收。请回答下列问题:
2SO3(g)+Q (Q>0),将SO2转化为SO3,尾气SO2可用NaOH溶液进行吸收。请回答下列问题: bB(g)+cC(g) 达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,A的浓度变为原来的40%,则( )
bB(g)+cC(g) 达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,A的浓度变为原来的40%,则( )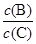 将 (填“增大”、“减小”或“不变”)。
将 (填“增大”、“减小”或“不变”)。 2NH3(g)
2NH3(g)