题目内容
【题目】元素周期表的一部分,回答下列问题(用元素符号填写):
族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | VIIA | O |
2 | ① | ② | ③ | ④ | ||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)分别写出①、③两种元素形成的高价态化合物的结构式
(2)写出⑨的原子结构示意图 .
(3)在这些元素中,最活泼的金属元素的最高价氧化物对应水化物的电子式 , 其溶于水时破坏的作用力为
(4)这些元素的最高价氧化物的对应水化物中酸性最强;形成的两性氢氧化物的化学式是;上述两者反应的离子方程式
(5)从⑤到的元素中,原子半径最小 .
【答案】
(1)O=C=O
(2)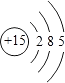
(3)![]() ;离子键
;离子键
(4)HClO4;Al(OH)3;Al(OH)3+3H+═Al3++3H2O
(5)Cl
【解析】解:由元素在周期表中位置,可知①为C、②为N、③为O、④为F、⑤为Na、⑥为Mg、⑦为Al、⑧为Si、⑨为P、⑩为S、为Cl、为Ar.(1)①、③两种元素形成的高价态化合物为二氧化碳,其结构式为O=C=O,所以答案是:O=C=O;(2)P的原子结构中有3个电子层,最外层电子数为5,⑨的原子结构示意图为 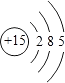 ,所以答案是:
,所以答案是: 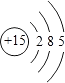 ;(3)最活泼金属为Na,最高价氧化物对应水化物为NaOH,电子式为
;(3)最活泼金属为Na,最高价氧化物对应水化物为NaOH,电子式为 ![]() ,溶于水电离出钠离子和氢氧根离子,则溶于水时破坏的作用力为离子键,所以答案是:
,溶于水电离出钠离子和氢氧根离子,则溶于水时破坏的作用力为离子键,所以答案是: ![]() ;离子键;(4)这些元素的最高价氧化物的对应水化物中酸性最强的为HClO4;形成的两性氢氧化物的化学式是Al(OH)3;上述两者反应的离子方程式为Al(OH)3+3H+═Al3++3H2O,所以答案是:HClO4;Al(OH)3;Al(OH)3+3H+═Al3++3H2O;(5)电子层越少,半径越小;同周期原子序数大的原子半径小,则从⑤到的元素中,原子半径最小Cl,所以答案是:Cl.
;离子键;(4)这些元素的最高价氧化物的对应水化物中酸性最强的为HClO4;形成的两性氢氧化物的化学式是Al(OH)3;上述两者反应的离子方程式为Al(OH)3+3H+═Al3++3H2O,所以答案是:HClO4;Al(OH)3;Al(OH)3+3H+═Al3++3H2O;(5)电子层越少,半径越小;同周期原子序数大的原子半径小,则从⑤到的元素中,原子半径最小Cl,所以答案是:Cl.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案
相关题目