题目内容
【题目】下列物质中:①NaCl;②NaOH;③NH3·H2O;④CH3COOH溶液;⑤BaSO4;⑥H2O;⑦HCl;⑧H2SO4;⑨CO2;⑩酒精溶液(均填写编号回答)
(1)pH相等的②的溶液和③的溶液等体积加水稀释相同倍数后,pH大的是______.
(2)有pH均为2的④、⑦、⑧三种物质的溶液,物质的量浓度大到小的顺序为______,若分别用这三种酸中和含等物质的量NaOH的溶液,所需酸溶液的体积分别为a、b、c,则a、b、c的大小关系是__________.
(3)某温度时,1mol·L-1的醋酸溶液电离平衡常数为1.0×10-8,达平衡时,溶液中氢离子浓度是______________.
【答案】 ③ ④>⑦>⑧ b=c>a 1.0×10-4mol·L-1
【解析】(1)一水合氨是弱电解质,在水溶液中存在电离平衡,加水稀释时,氢氧根离子物质的量增大,NaOH是强电解质,加水稀释时氢氧根离子物质的量不变,加水稀释相同倍数后,一水合氨溶液中氢氧根离子物质的量浓度大,pH大,故答案为③;(2)醋酸是一元弱酸,盐酸是一元强酸,硫酸是二元强酸,pH相同时,醋酸浓度大于盐酸,盐酸浓度大于硫酸;pH相同时,氢离子浓度相同,醋酸不完全电离,醋酸浓度远远大于盐酸和硫酸,若分别用pH相等的这三种酸中和含等物质的量NaOH的溶液,所需酸溶液的体积醋酸<盐酸=硫酸,故答案为:④>⑦>⑧;b=c>a;(3)醋酸的电离方程式为:CH3COOHH++CH3COO-,其平衡常数表达式为K=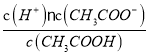 ;c2(H+)=Kc(CH3COOH) =1.0×10-8×1mol/L=1.0×10-8mol/L,c(H+)=1.0×10-4mol/L。
;c2(H+)=Kc(CH3COOH) =1.0×10-8×1mol/L=1.0×10-8mol/L,c(H+)=1.0×10-4mol/L。

【题目】二氧化锆(ZrO2)是最重要的氧离子固体电解质,用于制造燃料电池、氧气含量测定仪等。可由锆英砂(主要成分为ZrSiO4,也可表示为ZrO2·SiO2;含有少量Fe2O3、Al2O3、SiO2杂质)通过如工艺流程法制得。
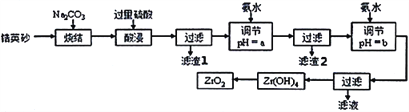
已知:①ZrO2具有两性,高温与纯碱共熔生成可溶于水的Na2ZrO3,与酸反应生成ZrO2+。
②部分金属离子在实验条件下开始沉淀和完全沉淀的pH如下表。
金属离子 | Fe3+ | Al3+ | ZrO2+ |
开始沉淀时pH | 1.9 | 3.3 | 6.2 |
沉淀完全时pH | 3.2 | 5.2 | 8.0 |
请回答下列问题:
(1)已知Zr元素的原子序数是40,请写出它在周期表中的位置:____________________________。
(2)烧结时ZrSiO4发生反应的化学方程式为__________________________;滤渣1的化学式为__________。
(3)调节pH=a时,a的范围应该是__________________;用氨水调节pH=b时,所发生反应的离子方程式为_______________________________________。
(4)本题的流程中,一共有三步过滤操作,北中最后一步过滤所得的Zr(OH)4沉淀需要洗涤,证明该沉淀已经洗涤干净的最佳操作方法是:______________________________________。
(5)工业上用铝热法冶炼锆,写出以ZrO2通过铝热法制取锆的化学方程式:________________。
(6)一种新型燃料电池用掺杂Y2O3的ZrO2晶体作电解质在熔融状态下传导O2-,一极通入空气,另一极通入乙烷,写出负极的电极反应式:________________________________。