题目内容
(1)写出下列反应的化学方程式:
①铝热反应(铝粉与四氧化三铁): ;②铜片与过量的浓硫酸共热: ;
(2)写出下列反应的离子方程式:
③铵盐溶液与烧碱溶液共热: ;④铜片与浓硝酸反应: .
①铝热反应(铝粉与四氧化三铁):
(2)写出下列反应的离子方程式:
③铵盐溶液与烧碱溶液共热:
考点:铝的化学性质,铵盐,硝酸的化学性质,浓硫酸的性质
专题:离子反应专题,元素及其化合物
分析:(1)①反应生成氧化铝和铁;
②反应生成硫酸铜、二氧化硫和水;
(2)③实质为铵根离子与氢氧根离子反应生成氨气和水;
④反应生成硝酸铜、NO和水,部分硝酸根离子不参加反应.
②反应生成硫酸铜、二氧化硫和水;
(2)③实质为铵根离子与氢氧根离子反应生成氨气和水;
④反应生成硝酸铜、NO和水,部分硝酸根离子不参加反应.
解答:
解:(1)①铝粉与四氧化三铁发生的铝热反应为8Al+3Fe3O4
4Al2O3+9Fe,故答案为:8Al+3Fe3O4
4Al2O3+9Fe;
②铜片与过量的浓硫酸共热的反应为Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O,故答案为:Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O;
(2)③铵盐溶液与烧碱溶液共热的离子反应为NH4++OH-
NH3↑+H2O,故答案为:NH4++OH-
NH3↑+H2O;
④铜片与浓硝酸反应反应的离子反应为Cu+4H++2NO3-═Cu2++2NO2↑+2H2O,故答案为:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O.
| ||
| △ |
| ||
| △ |
②铜片与过量的浓硫酸共热的反应为Cu+2H2SO4(浓)
| ||
| ||
(2)③铵盐溶液与烧碱溶液共热的离子反应为NH4++OH-
| ||
| ||
④铜片与浓硝酸反应反应的离子反应为Cu+4H++2NO3-═Cu2++2NO2↑+2H2O,故答案为:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O.
点评:本题考查Al的化学性质及离子反应、化学反应的书写,为高频考点,把握发生的反应为解答的关键,侧重化学用语书写的考查,题目难度不大.

练习册系列答案
 天天向上口算本系列答案
天天向上口算本系列答案
相关题目
X、Y分别是两种药物,其结构如图.
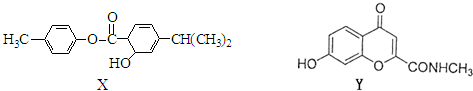
下列说法不正确的是( )
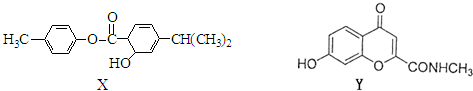
下列说法不正确的是( )
| A、1mol X与NaOH溶液反应,最多消耗2 mol NaOH |
| B、X、Y都有较强的水溶性 |
| C、X、Y都能使KMnO4溶液褪色 |
| D、X、Y的水解产物有可能发生聚合反应 |
下列说法不正确的是( )
| A、在一定条件下,催化分解80g SO3,混合气体中氧原子数为3×6.02×1023 |
| B、一定条件下,铁与水蒸气反应生成8.96L H2时(已折合成标况),转移的电子数为0.8×6.02×1023 |
| C、100mL 1mol/L AlCl3与3mol/L NaCl的混合溶液中,Cl-的个数为0.6×6.02×1023 |
| D、含有非极性键的数目为6.02×1023的Na2O2与水充分反应,标况下产生O2 22.4L |
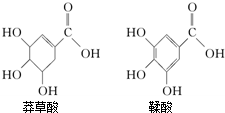 莽草酸是一种合成治疗禽流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中.下列关于这两种有机化合物(如图)的说法正确的是( )
莽草酸是一种合成治疗禽流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中.下列关于这两种有机化合物(如图)的说法正确的是( )| A、两种酸都能与溴水发生反应 |
| B、鞣酸分子与莽草酸分子相比多了两个碳碳双键 |
| C、1mol莽草酸完全燃烧消耗7mol O2 |
| D、等物质的量的两种酸与足量氢氧化钠反应,消耗氢氧化钠的量相同 |