题目内容
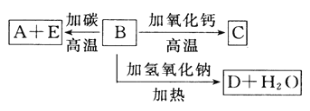
【题目】A、B、C、D、E代表单质或化合物,它们之间的相互转换关系如下图所示。A为地壳中含量仅次于氧的非金属元素的单质。
请填空:
(1)形成单质A的原子的结构示意图为______,它的最高化合价为______。
(2)B的化学式(分子式)为______,B和碳反应生成A和E的化学方程式是____________。
(3)C的化学式(分子式)为___________,D的化学式(分子式)为_____________。
【答案】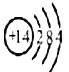 +4 SiO2 SiO2+2C
+4 SiO2 SiO2+2C![]() Si+2CO↑ CaSiO3 Na2SiO3
Si+2CO↑ CaSiO3 Na2SiO3
【解析】
A为地壳中含量仅次于氧的非金属元素的单质,可确定A是Si单质,它可由SiO2和C在高温条件下反应制取,则B为SiO2,E为CO,C为CaSiO3,D为Na2SiO3,结合对应的物质的性质以及题目要求可解答该题。
根据上述分析可知A是Si单质,B是SiO2,C为CaSiO3,D为Na2SiO3,E为CO。
(1)Si是14号元素,形成单质A的原子结构示意图为 ;Si原子最外层有4个电子,由于原子最外层电子数等于该元素的最高正化合价,所以Si元素的最高正化合价为+4价;
;Si原子最外层有4个电子,由于原子最外层电子数等于该元素的最高正化合价,所以Si元素的最高正化合价为+4价;
(2)根据上述推断可知B为二氧化硅,B的化学式为SiO2;
二氧化硅和碳在高温下反应生成硅单质和一氧化碳,反应的化学方程式是:SiO2+2C![]() Si+2CO↑;
Si+2CO↑;
(3)C是硅酸钙,化学式为CaSiO3;D为硅酸钠,其化学式Na2SiO3。

 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案【题目】下列实验操作、实验现象和实验结论均正确的是( )
选项 | 实验操作 | 实验现象 | 实验结论 |
A | 将Al2(SO4)3溶液和NaHCO3溶液混合 | 产生白色沉淀,并有大量气体生成 | 生成Al2(CO3)3沉淀和CO2气体 |
B | 在淀粉溶液中加入几滴稀硫酸,水浴5min,加入NaOH溶液调溶液pH至碱性,再加入新制的Cu(OH)2悬浊液,加热 | 有红色沉淀生成 | 淀粉完全水解 |
C | 将少量SO2气体通过足量Na2O2 | 余下气体能使带火星木条复燃 | 有O2生成 |
D | 用pH试纸分别测定等浓度的A、B两溶液(可能为NaHCO3或者Na2CO3)的pH值 | pHA> pHB | A溶液为Na2CO3溶液 |
A. A B. B C. C D. D
【题目】用下列实验装置进行相应的实验,不能达到实验目的的是
A | B | C | D | |
装置 |
|
|
|
|
实验 | 结合秒表定量比较锌与不同浓度的稀硫酸反应的快慢 | 证明温度对化学平衡的影响 | 验证铁钉发生吸氧腐蚀 | 可证明非金属性Cl>C>Si |
A. A B. B C. C D. D