题目内容
20.人类利用有机化合物满足生产生活各个方面的需求,下列有关叙述正确的是( )| A. | 煤的干馏属于物理变化 | |
| B. | 油脂在酸性或碱性条件下的水解反应叫做皂化反应 | |
| C. | 石油分馏得到的各馏分都是纯净物 | |
| D. | 淀粉和纤维素在一定条件下水解均可得到葡萄糖 |
分析 A.物理变化无新物质生成,煤的干馏有新物质生成;
B.油脂在碱性条件下水解出硬质酸钠和甘油为皂化反应;
C.石油的各种馏分仍然是混合物;
D.淀粉和纤维素均为多糖,为葡萄糖的脱水缩合物.
解答 解:A.煤的干馏指煤在隔绝空气条件下加热、分解,生成焦炭(或半焦)、煤焦油、粗苯、煤气等产物的过程,有新物质生成,属于化学变化,故A错误;
B.肥皂的主要成分是硬质酸钠,而油脂只有在碱性条件下水解才能水解出硬质酸钠,在酸性条件下水解出硬脂酸,故油脂在碱性条件下的水解才称为皂化反应,故B错误;
C.石油的各种馏分仍然是多种烷烃和环烷烃的混合物,无固定熔沸点,故C错误;
D.淀粉和纤维素均为葡萄糖的脱水缩合物,故淀粉和纤维素水解后均得葡萄糖,故D正确;
故选D.
点评 本题考查了化学在生产和生活中的应用,题目难度不大,应注意的是煤的干馏是化学变化,而石油的分馏是物理变化.

练习册系列答案
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案
相关题目
5.某元素的原子最外层只有一个电子,它与ⅦA元素结合时形成的化学键的说法正确的是( )
| A. | 一定是共价键 | B. | 一定是离子键 | ||
| C. | 可能是共价键,也可能是离子键 | D. | 以上说法都不正确 |
11.设NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 标准状况下,22.4LCH4和CH2C12的混合物所含分子数为NA | |
| B. | 用含0.2mo1 FeC13的饱和溶液制得胶体,其中所含氢氧化铁胶粒的数目为0.2 NA | |
| C. | 由NO2和CO2组成的混合气体中共有NA个分子,其中氧元素的质量一定为32g | |
| D. | 2LpH=1的HA酸溶液与足量锌粒反应,生成H2的分子数一定为0.1 NA |
8.以赤铁矿(化学成分为Fe2O3)为原料,经铝热反应所得的熔融物一般是铁铝合金,查阅《化学手册》得知,Al、Al2O3、Fe、Fe2O3熔点,沸点数据如下:
请回答下列问题:
(1)写出铝热反应的化学方程式:2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3;
(2)从表中数据推测铝热反应所得到的熔融物是铁铝合金的理由:Al的熔点比Fe的低;
(3)根据已有知识写出一种验证产物中有Fe的最简单方法:用磁铁吸引,如果能吸引,说明有铁生成;
(4)设计一个简单的实验方案,证明上述所得的熔融物中含有金属铝.(只用反应离子方程式表示):2Al+2OH-+2H2O=2AlO2-+3H2↑;
(5)在铝热反应中,若铝粉用得过多,在反应后还可回收到铝和氧化铝的混合物,假设针15g该混合物加入150mL稀硫酸中,在标准状况下放出1.68L氢气,为中和过量的硫酸,并使溶液中的Al3+恰好完全转化为Al(OH)3沉淀,需要200mL浓度为6mol•L-1的NaOH溶液,同该稀硫酸的物质的量浓度是4mol/L.
| 物质 | Al | Al2O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2054 | 1535 | 1462 |
| 沸点/℃ | 2467 | 2980 | 2750 |
(1)写出铝热反应的化学方程式:2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3;
(2)从表中数据推测铝热反应所得到的熔融物是铁铝合金的理由:Al的熔点比Fe的低;
(3)根据已有知识写出一种验证产物中有Fe的最简单方法:用磁铁吸引,如果能吸引,说明有铁生成;
(4)设计一个简单的实验方案,证明上述所得的熔融物中含有金属铝.(只用反应离子方程式表示):2Al+2OH-+2H2O=2AlO2-+3H2↑;
(5)在铝热反应中,若铝粉用得过多,在反应后还可回收到铝和氧化铝的混合物,假设针15g该混合物加入150mL稀硫酸中,在标准状况下放出1.68L氢气,为中和过量的硫酸,并使溶液中的Al3+恰好完全转化为Al(OH)3沉淀,需要200mL浓度为6mol•L-1的NaOH溶液,同该稀硫酸的物质的量浓度是4mol/L.
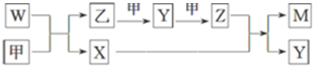
5.A、B、D、E四种元素均为短周期元素,原子序数逐渐增大,A元素原子的核外电子数、电子层数和最外层电子数均相等,B、D、E三种元素在周期表中的相对位置如图①所示,只有E元素的单质能与水反应生成两种酸.甲、乙、M、W、X、Y、Z七种物质均由A、B、D三种元素中的一种或几种组成,其中只有M分子同时含有三种元素;W为A、B两元素组成的10电子分子,溶于水显碱性;甲、乙为非金属单质;X分子含有10个电子,常温下为无色液体.它们之间的转化关系如图②所示.已知W和甲反应生成乙和X是置换反应,
请回答下列问题:
(1)W的电子式为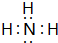
(2)甲和乙反应生成标准状况下1.12LY,吸收9.025kJ的热量,写出该反应的热化学方程式N2(g)+O2(g)=2NO(g)△H=+361kJ/mol
(3)用石墨做电极电解NaE溶液的离子方程式为2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$H2↑+Cl2↑+2OH-
(4)将一定量的A2、B2的混合气体放入1L密闭容器中,在500℃、2×107Pa下达到平衡.测得平衡气体的总物质的量为0.50mol,其中A2为0.3mol,B2为0.1mol.平衡转化率指某一可逆化学反应达到平衡状态时,转化为目的产物的某种原料量占该种原料起始量的百分数,则该条件下A2的平衡转化率为33.3%.
请回答下列问题:
| B | D | |
| E |

(1)W的电子式为
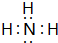
(2)甲和乙反应生成标准状况下1.12LY,吸收9.025kJ的热量,写出该反应的热化学方程式N2(g)+O2(g)=2NO(g)△H=+361kJ/mol
(3)用石墨做电极电解NaE溶液的离子方程式为2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$H2↑+Cl2↑+2OH-
(4)将一定量的A2、B2的混合气体放入1L密闭容器中,在500℃、2×107Pa下达到平衡.测得平衡气体的总物质的量为0.50mol,其中A2为0.3mol,B2为0.1mol.平衡转化率指某一可逆化学反应达到平衡状态时,转化为目的产物的某种原料量占该种原料起始量的百分数,则该条件下A2的平衡转化率为33.3%.
12.下列关于Na元素的叙述中,不正确的是( )
| A. | Na原子最外层有1个电子 | B. | Na单质能跟水反应放出氢气 | ||
| C. | Na原子比Mg原子更易失去电子 | D. | Na与氧气在加热条件下生成氧化钠 |
9.下列物质的变化是通过消去反应实现的是( )
| A. | CH2=CH2→CH3CH2Cl | B. | CH≡CH→CH3-CH3 | ||
| C. | CH3CH2OH→CH2=CH2 | D. | 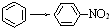 |
10.对下列各组反应所属类型的判断和书写均正确的是( )
| A. | CaC2与水反应制乙炔,乙烯与水反应制乙醇--水解反应 | |
| B. | 由苯制硝基苯,由甲苯制TNT--消化反应 | |
| C. | 油脂的硬化,油脂的氢化--加聚反应 | |
| D. | 乙醇与酸性K2Cr2O7溶液反应,乙醛与新制Cu(OH)2浊液反应--氧化反应 |