题目内容
现有①BaCl2、②金刚石、③KOH、④Na2SO4、⑤干冰、⑥碘六种物质,按下列要求回答问题.
(1)熔化时不需要破坏化学键的是 (填写物质的序号,下同),熔化时需要破坏共价键的是 .
(2)属于离子化合物的是 ,只有离子键的物质是 .
(1)熔化时不需要破坏化学键的是
(2)属于离子化合物的是
考点:离子化合物的结构特征与性质,不同晶体的结构微粒及微粒间作用力的区别
专题:化学键与晶体结构
分析:(1)分子晶体熔化不需要破坏化学键;金属晶体、原子晶体、离子晶体熔化时需要破坏化学键;
(2)含有离子键的化合物为离子化合物,活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键.
(2)含有离子键的化合物为离子化合物,活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键.
解答:
解:(1)分子晶体熔化不需要破坏化学键;金属晶体、原子晶体、离子晶体熔化时需要破坏化学键,所以熔化时不需要破坏化学键的是干冰和碘,熔化时需要破坏化学键的是氯化钡、金刚石、KOH、硫酸钠,故答案案为:⑤⑥;①②③④;
(2)含有离子键的化合物为离子化合物,活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,所以属于离子化合物的有①③④;只含离子键的为①,
故答案为:①③④;①.
(2)含有离子键的化合物为离子化合物,活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,所以属于离子化合物的有①③④;只含离子键的为①,
故答案为:①③④;①.
点评:本题考查了离子键、化合物类型的判断等知识点,根据物质的构成微粒及微粒间的作用力分析解答即可,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列离子方程式中书写正确的是( )
| A、FeCl2溶液中通入Cl2 Fe2++Cl2═Fe3++2Cl- |
| B、SiO2与NaOH溶液反应 SiO2+2OH-+2Na+═Na2SiO3+H2↑ |
| C、FeCl3溶液与铜 Fe3++Cu═Fe2++Cu2+ |
| D、用稀硫酸除去铁锈 Fe2O3+6H+═2Fe3++3H2O |
对甲基苯甲酸(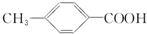 )是一种广泛应用于制备止血芳酸、农药杀虫剂、感光材料的白色晶体,已知其有多种同分异构体,其中属于酯类(分子结构形式为:
)是一种广泛应用于制备止血芳酸、农药杀虫剂、感光材料的白色晶体,已知其有多种同分异构体,其中属于酯类(分子结构形式为: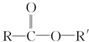 ,R为烃基或H,R′为烃基),且分子结构中含有甲基和苯环的同分异构体的种数为( )
,R为烃基或H,R′为烃基),且分子结构中含有甲基和苯环的同分异构体的种数为( )
 )是一种广泛应用于制备止血芳酸、农药杀虫剂、感光材料的白色晶体,已知其有多种同分异构体,其中属于酯类(分子结构形式为:
)是一种广泛应用于制备止血芳酸、农药杀虫剂、感光材料的白色晶体,已知其有多种同分异构体,其中属于酯类(分子结构形式为: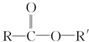 ,R为烃基或H,R′为烃基),且分子结构中含有甲基和苯环的同分异构体的种数为( )
,R为烃基或H,R′为烃基),且分子结构中含有甲基和苯环的同分异构体的种数为( )| A、3种 | B、4种 | C、5种 | D、6种 |
下列物质的包装箱应贴上如图标识的是( )


| A、纯碱 | B、汽油 | C、浓硫酸 | D、氨水 |

 在常温常压下,可利用下列装置来测定气体体积,抽气装置E用以调节装置中的气压差,减小实验误差.
在常温常压下,可利用下列装置来测定气体体积,抽气装置E用以调节装置中的气压差,减小实验误差.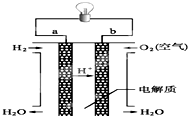 人们应用原电池原理制作了多种电池,以满足不同的需要.以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格.
人们应用原电池原理制作了多种电池,以满足不同的需要.以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格.