题目内容
16.下列有关物质用途的说法中,不正确的是( )| A. | 晶体硅可用于制作光导纤维 | B. | 过氧化钠可作潜水艇中的供氧剂 | ||
| C. | 氢氟酸可用来刻蚀玻璃 | D. | 漂白粉可用作游泳池的消毒剂 |
分析 A.光导纤维的成分是二氧化硅;
B.氧化钠与二氧化碳反应生成碳酸钠,生成氧气;
C.氢氟酸与二氧化硅反应,可以用来刻蚀玻璃;
D.漂白粉具有强氧化性,可以杀菌消毒.
解答 解:A.光导纤维的成分是二氧化硅,不是硅单质,故A错误;
B.过氧化钠与二氧化碳反应生成碳酸钠与氧气,过氧化钠可以用作潜水艇中的供氧剂,故B正确;
C.玻璃含有二氧化硅,氢氟酸与二氧化硅反应生成四氟化硅与氢气,可以用来刻蚀玻璃,故C正确;
D.漂白粉具有强氧化性,可以杀菌消毒,可用作游泳池的消毒剂,故D正确,
故选A.
点评 本题考查钠、硅及卤素化合物性质与用途,比较基础,旨在考查学生对基础知识的理解掌握,注意基础知识的识记积累.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
7.下列关于物质的性质和用途的叙述中,不正确的是( )
| A. | 硅胶吸附能力很强,常用作袋装食品、瓶装药品的干燥剂 | |
| B. | 氧化铝熔点很高,可用来制作耐火坩埚及耐高温实验仪器 | |
| C. | 二氧化硫能使品红溶液褪色,将氯气通入二氧化硫的饱和溶液中可增强其漂白性 | |
| D. | 硅导电性介于导体和绝缘体之间,是良好的半导体材料 |
11.下列关于SO2的叙述中,正确的是( )
| A. | SO2的摩尔质量是64g | |
| B. | 1molSO2中含氧原子数约为6.02×1023 | |
| C. | 常温常压下,1molSO2的体积为22.4L | |
| D. | 常温常压下,64gSO2的物质的量为1mol |
8.已知碱能除去硝酸尾气:NO+NO2+2NaOH═2NaNO2+H2O、2NO2+2NaOH═NaNO2+NaNO3+H2O,根据硝酸尾气处理的反应原理,下列气体中不能被过量NaOH溶液吸收的是( )
| A. | 1mol O2和4mol NO2 | B. | 1mol O2和4mol NO | ||
| C. | 1mol NO和5mol NO2 | D. | 4mol NO和1mol NO2 |
14.乙烯(C2H4)、乙酸(C2H4O2)和甲醛(CH2O)组成的混合物中,氧元素的质量分数是37%,则碳元素的质量分数为( )
| A. | 27% | B. | 28% | C. | 54% | D. | 无法计算 |
15.设NA表示阿伏加德罗常数,下列说法中不正确的是( )
| A. | 53g Na2C03固体中含有的离子数总数为1.5NA | |
| B. | 78 g Na2O2与足量的水充分反应,转移的电子数目为NA | |
| C. | 46 g NO2 和 N2O4混合气体中含有原子数为3NA | |
| D. | 在标准状况下,22.4 L SO3中含原子数为4 NA |
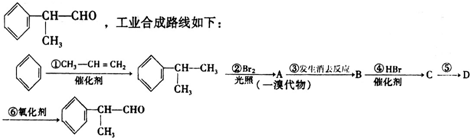
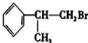 或
或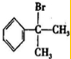 .
.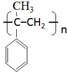 .
.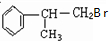 +NaOH$→_{△}^{H_{2}O}$NaBr+
+NaOH$→_{△}^{H_{2}O}$NaBr+ ,其反应类型为取代反应.
,其反应类型为取代反应. (或
(或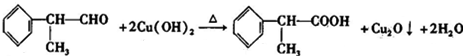 ).
).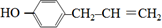 、
、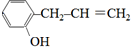 、
、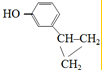 .
.