题目内容
5.已知723K时,2SO2(g)+O2(g)?2SO3(g)△H=-Q,在相同条件下,向一密闭容器中通入2mol SO2和1mol O2,达到平衡时放出的热量为Q1;向另一体积相同的密闭容器中通入1mol SO2和0.5mol O2,达到平衡时放出的热量为Q2.则Q1、Q2、Q满足的关系是( )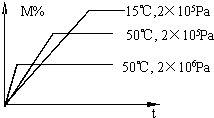
| A. | Q=2Q2 | B. | Q1=2Q2 | C. | Q=Q1>Q2 | D. | Q>Q1>Q2 |
分析 2SO2(g)+O2(g)?2SO3(g)△H=-QkJ/mol,表示在上述条件下2mol SO2和1molO2完全反应生成1molSO3气体放出热量为QkJ,再结合可逆反应中反应物不能完全反应及物质的量与放出的热量成正比、平衡移动等解答.
解答 解:反应的热化学方程式为:2SO2(g)+O2(g)?2SO3(g)△H=-Q kJ/mol,
由热化学方程式可知,在上述条件下反应生成2molSO3气体放热Q kJ,加入2mol SO2和1molO2,生成的三氧化硫量小于2mol,所以Q1<Q kJ,
通入1mol SO2和0.5molO2,如果转化率与加入2mol SO2和1molO2相同,则放热为$\frac{Q{\;}_{1}}{2}$kJ,但是此时体系压强比加入2mol SO2和1molO2要小,所以平衡会向左移动,所以实际放出的热量<$\frac{Q{\;}_{1}}{2}$kJ,即2Q2<Q1,综上得:2Q2<Q1<Q kJ,
故选D.
点评 本题考查平衡移动及反应热的计算,题目难度中等,本题注意浓度对平衡的影响以及可逆反应的特征.

练习册系列答案
相关题目
15.下列文字表述与反应方程式对应且正确的是( )
| A. | 溴乙烷中滴入AgNO3溶液检验其中的溴元素:Br-+Ag+═AgBr | |
| B. | 乙醛溶液中加入足量的银氨溶液并加热CH3CHO+2$Ag(N{H}_{3}{)_{2}}^{+}$$\stackrel{水溶加热}{→}$$C{H}_{3}CO{O}^{-}$+$N{H}_{4}^{+}$+3NH3+2Ag↓+H2O | |
| C. | 向苯酚钠溶液中通入少量二氧化碳CO2+H2O+2C6H5O-→2C6H5OH+CO32- | |
| D. | 实验室用浓溴水检验苯酚: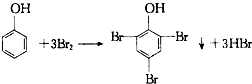 |
13.下列说法正确的是( )
| A. | 药品柜的同一层不可存放浓硝酸和浓氨水 | |
| B. | 保存在无色玻璃试剂瓶中的浓硝酸要放在阴凉处 | |
| C. | 铵态氮肥可与草木灰混合雨天施用 | |
| D. | 固氮就是将氮元素转化成固体 |
10.NA为阿伏伽德罗常数,下列叙述错误的是( )
| A. | 17gNH3中含有的质子数为10NA | |
| B. | 12g金刚石中含有的共价键数为4 NA | |
| C. | 46gNO2和N2O4混合气体中含有的原子总数为3 NA | |
| D. | 1molNa与足量的O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子 |
17.已知短周期元素的离子aA2+、bB+、cC2-、dD-都具有相同的核外电子排布,则下列叙述正确的是( )
| A. | 原子半径D<C<B<A | B. | 原子序数 d>c>a>b | ||
| C. | 离子半径C>D>B>A | D. | 单质的氧化性C>D>A>B |
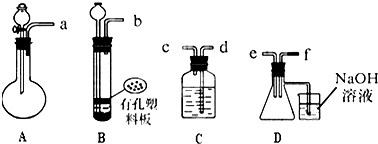
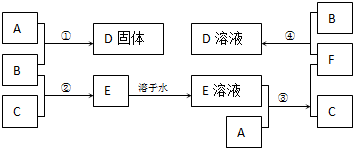 室温下,单质A、B、C分别为固体、黄绿色气体、无色气体,在合适的反应条件下,它们可以按下面的框图进行反应.又知E溶液是无色的.
室温下,单质A、B、C分别为固体、黄绿色气体、无色气体,在合适的反应条件下,它们可以按下面的框图进行反应.又知E溶液是无色的.