题目内容
某种稀H2SO4和稀HNO3混合溶液100mL,其中,C(H+)=1 mol?L-1, C(NO3-)=0.2 mol?L-1。
(1)计算C(SO42-) (2分)
(2)若往上述混酸溶液中加入足量铜片,可生成标准状况下的气体多少升? (4分)
(1)C(SO42-)=(1 mol?L-1-0.2 mol?L-1)/2=0.4 mol?L-1。(2分)
(2)根据:3Cu + 8H+ + 2NO3-= 3Cu2+ +2NO↑ + 4H2O
∵ n (H+) :n (NO3-)=0.1 mol :0.02 mol > 4 :1,∴H+ 过量。(2分)
则n (NO)=n (NO3-)=0.02 mol,V(NO)=0.448L。 (2分)

练习册系列答案
相关题目
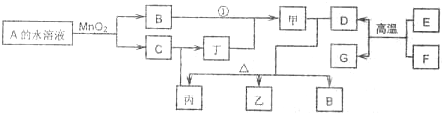
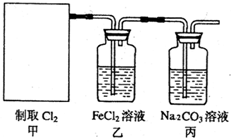 (2011?南京模拟)氯气是一种重要的化工原料.
(2011?南京模拟)氯气是一种重要的化工原料.