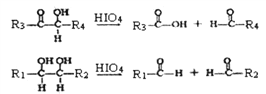
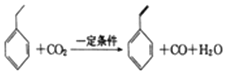
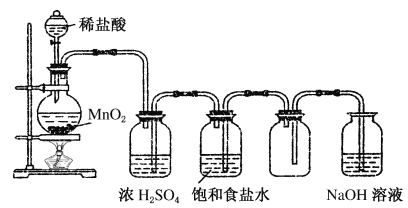
题目内容
【题目】电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
(1)检验溶液中Fe3+存在的试剂是_____,证明Fe3+存在的现象是__________。
(2)写出FeCl3溶液与金属铜发生反应的化学方程式:_________________。
(3)某工程师为了从使用过的腐蚀废液中回收铜,并重新获得纯净的FeCl3溶液,准备采用下列步骤:
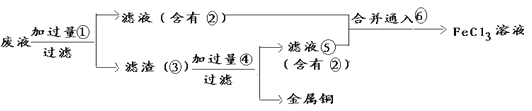
①请写出上述实验中③的化学式:_______
②配制并保存硫酸亚铁溶液时,常在其中加入_______________________
③要证明某溶液中不含Fe3+而可能含有Fe2+,进行如下实验操作时的最佳顺序为______。
①加入足量氯水 ②加入足量![]() 溶液 ③加入少量KSCN溶液
溶液 ③加入少量KSCN溶液
A、①③ B、③② C、③① D、①②③
④写出向②⑤的合并液中通入⑥的离子方程式__________________
【答案】KSCN溶液溶液变为红色2FeCl3+Cu=2FeCl2+ CuCl2Cu、Fe稀硫酸与铁粉C2Fe2++Cl2=2Fe3++2Cl-
【解析】
(1)常用于检验三价铁的试剂是KSCN溶液,现象为溶液变为红色。
(2)FeCl3溶液与金属铜反应生成铜离子和二价铁离子,反应方程式为:2FeCl3+Cu=2FeCl2+ CuCl2;
(3)①通过流程图可知单质铜来自于滤渣③,则第一步为置换单质铜,故过量物质①为Fe,滤渣③为Fe和Cu的混合物,滤液②为FeCl2溶液,分开滤渣③中的Fe和Cu,又要是滤液⑤与滤液②混合,所以过量的④为稀盐酸,滤液⑤也为FeCl2溶液,②、⑤混合最终要得到FeCl3溶液,则通入⑥为过量的Cl2;
②配置并保存硫酸亚铁溶液需考虑防止Fe2+水解及氧化,防止水解需加入稀硫酸,防止氧化需加入Fe粉;
③要证明某溶液中不存在Fe3+,而可能存在Fe2+则需先加入KSCN溶液现象溶液不变色,再通入过量的Cl2,若溶液变红则含有Fe2+,故选C;
④滤液②⑤为FeCl2溶液,通入氯气将Fe2+氧化为Fe3+,离子方程式为:2Fe2++Cl2=2Fe3++2Cl-。