��Ŀ����
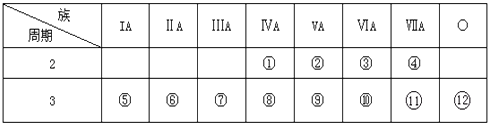
����Ŀ������������ȼ�ϵ�أ�SOFC���Թ�����������Ϊ����ʣ��乤��ԭ����ͼ��ʾ�����й��ڹ���ȼ�ϵ�ص��й�˵������ȷ���ǣ�������
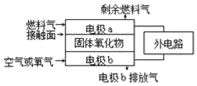
A. ������������������õ����ڵ����ͨ��
B. ������������O2����a����b���ƶ�
C. �缫bΪ��صĸ������缫��ӦʽΪ��O2+4e��=2O2��
D. ����C3H8Ϊȼ��������Ӵ����Ϸ����ķ�ӦΪC3H8��20e��+10O2���T3CO2+4H2O
���𰸡�D
��������A������ԭ��صĹ���ԭ��������ڲ�û�е��ӵ�ͨ����ֻ���������ӵ�ͨ������˹������������������������ͨ�����γɱպϻ�·���ʴ���B�����������ƶ����������������ƶ���ȼ�ϵ����ͨ���������һ��Ϊ������ͨȼ�ϵ�һ��Ϊ���������O2����b��a�ƶ����ʴ���C����������������bΪ�������缫��ӦʽΪO2��4e��=2O2�����ʴ���D��ȼ�ϵ���൱��ȼ�գ�ӦΪ����O2����C3H8��CO2��H2O�����ݻ��ϼ۵ı仯����ʧȥ����20e����C3H8��20e����3CO2��4H2Oǰ�����غ㡢ԭ���غ㣬��˵缫��ӦʽΪ��C3H8 �C 20e- + 10O2- =3CO2 +4H2O������ȷ��

 ����ȫ���ִʾ��ƪ��ϵ�д�
����ȫ���ִʾ��ƪ��ϵ�д� �����߿����ϵ�д�
�����߿����ϵ�д� �㾦�½̲�ȫ�ܽ��ϵ�д�
�㾦�½̲�ȫ�ܽ��ϵ�д�����Ŀ�����ݱ�����Ϣ���ж�������������ȷ����(��)
��� | ������ | ��ԭ�� | ������Ӧ�� | �������� | ��ԭ���� |
�� | Cl2 | FeBr2 | / | Fe3����Br2 | |
�� | KClO3 | Ũ���� | / | Cl2 | |
�� | KMnO4 | H2O2 | H2SO4 | O2 | Mn2�� |
A. �ɱ����������Ϣ��֪ͨ��Cl2������ͬ������������ܲ�ͬ
B. ��Ӧ���У���ֻ������Cl2ʱ����Ӧ�ɱ�ʾΪCl2�� Fe2��===Fe3���� 2Cl��
C. �������鷴Ӧ�Ļ�ԭ������KCl������ת����Ŀ��6e��
D. �������鷴Ӧ�����ӷ���ʽΪ2MnO![]() �� 3H2O2��6H��===2Mn2���� 4O2���� 6H2O
�� 3H2O2��6H��===2Mn2���� 4O2���� 6H2O