题目内容
将一定量Cl2通入250 mL KBr溶液中,反应后将溶液蒸干,测知所得的固体中含溴元素10 g,且K+与Cl-的物质的量比为2∶1。试求:
(1)通入Cl2的体积(标准状况)。
(2)原KBr溶液的物质的量浓度。
(1)通入Cl2的体积(标准状况)。
(2)原KBr溶液的物质的量浓度。
(1)1.4 L (2)1 mol·L-1
(1)固体中,n(Br?)=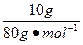 ="0.125" mol
="0.125" mol
由于n(K+)∶n(Cl-)=2∶1
根据电荷守恒:
n(K+)=n(Cl-)+n(Br-)
n(Cl-)=n(Br-)="0.125" mol
V(Cl2)=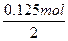 ×22.4 L·mol-1="1.4" L
×22.4 L·mol-1="1.4" L
(2)原n(KBr)=n(K+)="0.125" mol×2="0.25" mol,所以c(KBr)=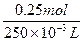 ="1" mol·L-1。
="1" mol·L-1。
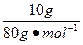 ="0.125" mol
="0.125" mol由于n(K+)∶n(Cl-)=2∶1
根据电荷守恒:
n(K+)=n(Cl-)+n(Br-)
n(Cl-)=n(Br-)="0.125" mol
V(Cl2)=
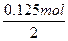 ×22.4 L·mol-1="1.4" L
×22.4 L·mol-1="1.4" L(2)原n(KBr)=n(K+)="0.125" mol×2="0.25" mol,所以c(KBr)=
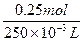 ="1" mol·L-1。
="1" mol·L-1。
练习册系列答案
相关题目
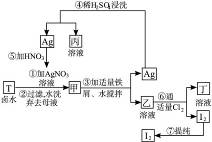
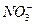
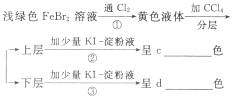
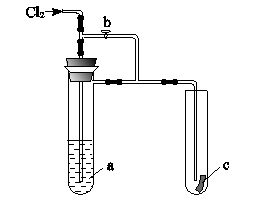
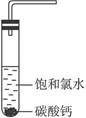
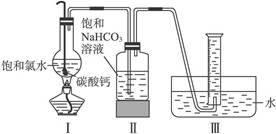
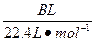 明显小于
明显小于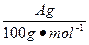 。若不考虑实验操作和CO2的溶解等因素造成的误差,从化学反应原理来看,导致这一大小关系的原因是____________________________________________。
。若不考虑实验操作和CO2的溶解等因素造成的误差,从化学反应原理来看,导致这一大小关系的原因是____________________________________________。