题目内容
【题目】中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%。减少CO2排放是一项重要课题。
(1)碳酸二甲酯(CH3OCOOCH3,简称DMC)是一种应用前景广泛的新材料,用甲醇、CO、CO2在常压、70~120 ℃和催化剂条件下合成DMC。
已知:①CO(g) +1/2O2(g) === CO2(g) ΔH1=-283.0 kJ·mol-1
②H2O(l)===H2O(g) ΔH2=+44.0 kJ·mol-1
③2CH3OH(g)+CO2(g) ![]() CH3OCOOCH3(g)+H2O(g) ΔH3=-15.5 kJ·mol-1
CH3OCOOCH3(g)+H2O(g) ΔH3=-15.5 kJ·mol-1
则2CH3OH(g)+CO(g)+1/2O2(g) ![]() CH3OCOOCH3(g)+H2O(l) ΔH=________。
CH3OCOOCH3(g)+H2O(l) ΔH=________。
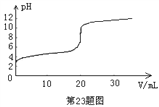
(2)在2L的密闭容器中通入2 mol CH3OH和1 mol CO2,按反应③合成DMC,一定条件下,平衡时CO2的转化率如图所示,则:

①A点的平衡常数为_________________
②v(A)、v(B)、v(C)由快到慢的顺序为__________________;
③下列能说明在此条件下反应达到平衡状态的是________。
A.2v正(CH3OH)=v逆(CO2)
B.CH3OH与CO2的物质的量之比保持不变
C.恒容条件,容器内气体的密度保持不变
D.各组分的物质的量分数保持不变
(3)CO2经催化加氢可以生成低碳烃,主要有以下两个竞争反应:
反应Ⅰ:CO2(g)+4H2(g) ![]() CH4(g)+2H2O(g)
CH4(g)+2H2O(g)
反应Ⅱ:2CO2(g)+6H2(g) ![]() C2H4(g)+4H2O(g)
C2H4(g)+4H2O(g)
为分析催化剂对反应的选择性,在1 L密闭容器中充入1 mol CO2和2 mol H2,测得有关物质的物质的量随温度变化如图所示。

①该催化剂在较低温度时主要选择________(填“反应Ⅰ”或“反应Ⅱ”)。
②用惰性电极电解强酸性的二氧化碳水溶液可得到乙烯,其原理如图所示。b电极上的电极反应式为________________________________。

【答案】-342.5 kJ·mol-1 1 v(C)>v(B)>v(A) D 反应Ⅰ 2CO2+12H++12e-===C2H4+4H2O
【解析】
(1)目标反应可由![]() 得到,根据盖斯定律,所求反应的焓变为
得到,根据盖斯定律,所求反应的焓变为![]() ,
,
故答案为:-342.5 kJ·mol-1;
(2)①A点的转化率为50%,列三段式,
则A点的平衡常数为![]() ;
;
②该反应为气体分子数减少的反应,压强越大转化率越高,故![]() ,A、B两点温度相同,C点温度最高,故
,A、B两点温度相同,C点温度最高,故![]() ;
;
③A、![]() ,正逆反应速率不相等,故A错;
,正逆反应速率不相等,故A错;
B、因甲醇和二氧化碳的初始投料比为2:1,反应消耗也是2:1,故甲醇和二氧化碳的物质的量之比始终是2:1,故甲醇与二氧化碳的物质的量之比保持不变无法判断反应是否是平衡状态,B错;
C、恒容时,总体积不变,根据质量守恒,气体总质量保持不变,故气体密度始终不变,无法判断是否平衡状态,C错;
D、各组分的物质的量分数保持不变,说明各组分的量不再变化,说明反应达到了平衡状态,D正确;
故答案为:1;![]() ;D;
;D;
(3)①根据图像,在温度低的时候,生成![]() 比
比![]() 要多,该催化剂在较低温度时主要选择反应Ⅰ;
要多,该催化剂在较低温度时主要选择反应Ⅰ;
②b电极连接电源负极,为阴极,发生还原反应,二氧化碳在酸性环境中转化为![]() ,故电极反应式为:
,故电极反应式为:![]() ;
;
故答案为:反应Ⅰ;![]() 。
。

【题目】己二酸是重要的有机合成中间体,是重要的化工原料。己二酸的物理常数如表所示:
物质 | 色态 | 相对分子质量 | 熔点/℃ | 溶解度(性) | |||
g/100mL水 | 乙醇 | ||||||
己二酸 | 白色晶体 | 146 | 152 | 15℃ | 25℃ | 100℃ | 易溶 |
1.4 | 2.3 | 160 | |||||
Ⅰ.制备己二酸的一种反应机理如下:
![]() +HNO3(浓)
+HNO3(浓)![]() HOOC(CH2)4COOH+NO2↑+H2O(未配平)
HOOC(CH2)4COOH+NO2↑+H2O(未配平)
制备己二酸的装置如图所示(夹持、加热装置省略)。

(1)向三颈烧瓶中加入2mL浓HNO3,再缓慢滴加1mL环己醇,保持80℃持续反应2h。仪器b的名称是______________,能否用于蒸馏冷凝: ____________(填“能”或“否”)。反应结束冷却至室温后,在冰水浴中冷却,分离出己二酸粗品,用冰水浴的目的是__________
(2)图中装置的缺陷为____________________。
Ⅱ.用浓HNO3做氧化剂的合成方法中,浓HNO3会严重腐蚀设备。科学家改进了合成已二酸的方法,改进后的反应机理如下:
![]()
![]() HOOC(CH2)4COOH
HOOC(CH2)4COOH
(环己烯,难溶于水,易溶于乙醇),使用的装置如图所示(夹持、加热装置省略)。

(3)仪器c与a相比较,优点在于___________。
(4)检验己二酸粗产品中含有少量环己烯时的方法_________。
(5)实验结束后,准确称取实验产品0.1500g于250mL锥形瓶中,加入50mL热的蒸馏水,搅拌溶解,滴加几滴酚酞。用0.1000molL-1 NaOH溶液滴定。重复上述操作两次,消耗NaOH的平均体积为20.00mL。
①滴定终点的现象为__________。
②产品的纯度为______________(保留3位有效数字)。