题目内容
4.氯水中存在Cl2+H2O?H++Cl-+HClO加入下列物质,能使HClO浓度增大的是( )| A. | NaCl | B. | NaHCO3 | C. | 浓H2SO4 | D. | Na2SO3 |
分析 能使HClO浓度增大,可加入与氢离子反应的物质,但不能与HClO反应,从而使Cl2+H2O?H++Cl-+HClO正向移动,以此来解答.
解答 解:A.加入氯化钠,氯离子浓度增大,平衡左移,次氯酸浓度降低,故A错误;
B.碳酸酸性弱于盐酸,次氯酸酸性弱于碳酸,所以加入碳酸氢钠,能够与氢离子反应,不能与次氯酸反应,平衡右移,次氯酸浓度增大,故B选;
C.加入浓硫酸,氢离子浓度增大,平衡左移,次氯酸浓度降低,故C错误;
D.加入亚硫酸钠溶液,能够与氯气反应,平衡左移,次氯酸浓度降低,故D错误;
故选:B.
点评 本题考查氯气的性质及平衡移动,明确物质的性质及化学平衡移动的影响因素是解题关键,题目难度不大.

练习册系列答案
相关题目
15.化学与生产、生活息息相关,下列叙述错误的是( )
| A. | 碱性锌锰干电池比普通锌锰干电池性能好,比能量和可储存时间均有提高 | |
| B. | 汽车加大油门、把食物放在冰箱里,食品包装袋内放置小包除氧剂,都是为了改变反应物转化率而采取的措施 | |
| C. | 1kg人体脂肪可存储约32 200kJ能量.一般人每行走1km 大约要消耗170kJ 能量,如果每天步行5km,一年(按365天计)中消耗的脂肪大约是9.6kg | |
| D. | 炒菜用铁锅未及时洗净(残液中含NaCl),可能发生电化学腐蚀生成红褐色锈斑 |
5.下列说法正确的是( )
| A. | 钠钾合金比纯钠的熔点高 | |
| B. | 鉴别碳酸氢钠中含有纯碱的方法是加热看是否有气体生成 | |
| C. | 水晶项链和餐桌上的瓷盘都是硅酸盐制品 | |
| D. | 太阳能电池板中的硅在元素周期表中处于金属与非金属的交界位置 |
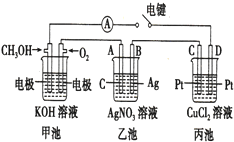 某兴趣小组的同学用如图所示装置研究有关电化学的问题,当闭合该装置的电键时,观察到电流的指针发生了偏转.
某兴趣小组的同学用如图所示装置研究有关电化学的问题,当闭合该装置的电键时,观察到电流的指针发生了偏转.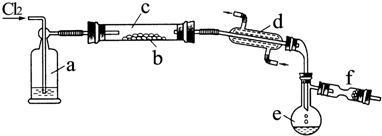
 .
.