题目内容
12..NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品中;NH4HSO4在分析试剂、医药、电子工业中用途广泛.请回答下列问题: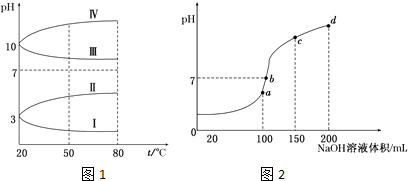
(1)NH4Al(SO4)2可作净水剂,其理由是Al3+水解生成的Al(OH)3胶体,具有吸附性,即Al3++3H2O?Al(OH)3胶体+3H+,Al(OH)3吸附悬浮颗粒使其沉降从而净化水
(用必要的化学用语和相关文字说明).
(2)相同条件下,0.1mol/L NH4Al(SO4)2中的c(NH${\;}_{4}^{+}$)小于(填“等于”、“大于”或“小于”)0.1mol/L NH4HSO4中的c(NH${\;}_{4}^{+}$).
(3)如图是0.1mol/L电解质溶液的pH随温度变化的图象.
①其中符合0.1mol/L NH4Al(SO4)2的pH随温度变化的曲线是Ⅰ(填写字母),导致pH随温度变化的原因是NH4Al(SO4)2水解,溶液呈酸性,升高温度,其水解程度增大,pH减小;
②20℃时,0.1mol/L NH4Al(SO4)2中2c(SO${\;}_{4}^{2-}$)-c(NH${\;}_{4}^{+}$)-3c(Al3+)=10-3 mol•L-1.
(4)室温时,向100mL 0.1mol/L NH4HSO4溶液中滴加0.1mol/L NaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示:试分析图中a、b、c、d四个点,水的电离程度最大的是a;在b点,溶液中各离子浓度由大到小的排列顺序是c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+).
分析 (1)Al3+水解生成的Al(OH)3胶体,具有吸附性;
(2)NH4Al(SO4)2水解,溶液呈酸性,NH4HSO4中的铵根离子水解显示酸性,根据铵根离子的水解程度来回答;
(3)①NH4Al(SO4)2水解,溶液呈酸性,升高温度其水解程度增大;②根据电荷守恒定律解题;①a、b、c、d四个点,根据反应量的关系,a点恰好消耗完H+,溶液中只有(NH4)2SO4与Na2SO4;
②b点溶液呈中性,即溶液含有(NH4)2SO4、Na2SO4、NH3•H2O三种成分,所以b点时c(Na+)>c(SO42-),根据N元素与S元素的关系,可以得出c(SO42-)>c(NH4+),据此分析.
(4)a、b、c、d四个点,根据反应量的关系,a点恰好消耗完H+,溶液中只有(NH4)2SO4与Na2SO4;b、c、d三点溶液均含有NH3•H2O,(NH4)2SO4可以促进水的电离,而NH3•H2O抑制水的电离.b点溶液呈中性;b点溶液为中性,溶质为(NH4)2SO4与Na2SO4、NH3•H2O,V(NaOH)>V(NH4HSO4).
解答 解:(1)Al3+水解生成的Al(OH)3胶体,具有吸附性,离子方程式:Al3++3H2O?Al(OH)3胶体+3H+,
故答案为:Al3+水解生成的Al(OH)3胶体,具有吸附性,即Al3++3H2O?Al(OH)3胶体+3H+,Al(OH)3吸附悬浮颗粒使其沉降从而净化水;
(2)NH4Al(SO4)2中铵根离子水解,溶液呈酸性,但是铝离子的存在抑制铵根离子的水解,NH4HSO4中的铵根离子水解显示酸性,但是氢离子对铵根离子的水解的抑制作用大于铝离子,所以0.1mol/L NH4Al(SO4)2中的铵根浓度小于0.1mol/L NH4HSO4中的铵根浓度,故答案为:小于;
(3)①NH4Al(SO4)2水解,溶液呈酸性,升高温度其水解程度增大,pH减小,符合的曲线为Ⅰ,
故答案为:1;NH4Al(SO4)2水解,溶液呈酸性,升高温度,其水解程度增大,pH减小;
②25℃时,0.1mol•L-1 NH4Al(SO4)2中PH=3,根据电荷守恒,阳离子所带的正电荷总数等于阴离子所带的负电荷总数,c(H+)+c(NH4+)+3c(Al3+)=c(OH-)+2c(SO42-),可以求出2c(SO42-)-c(NH4+)-3c(Al3+)=c(H+)-c(OH-)=10-3 mol•L-1[c(OH-)太小,可忽略],
故答案为:10-3 mol•L-1;
(4)a、b、c、d四个点,根据反应量的关系,a点恰好消耗完H+,溶液中只有(NH4)2SO4与Na2SO4;b、c、d三点溶液均含有NH3•H2O,(NH4)2SO4可以促进水的电离,而NH3•H2O抑制水的电离.b点溶液呈中性,所以a点水的电离程度最大,b点溶液为中性,溶质为(NH4)2SO4与Na2SO4、NH3•H2O,V(NaOH)>V(NH4HSO4),铵根离子水解,则离子浓度大小为c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+),故答案为:a;c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+).
点评 本题考查盐类的水解和离子浓度大小的比较、酸碱混合的定性判断,题目难度中等,注意根据守恒思想解题,注意把握反应的先后顺序为解答的关键,涉及盐类的水解和离子浓度大小的比较,题目难度较大,注意先发生中和后发生铵根离子与碱反应.

| A. | v(A)=3.0mol•L-1•min-1 | B. | v(B)=0.280 mol•L-1•s-1 | ||
| C. | v(C)=4.8mol•L-1•min-1 | D. | v(D)=0.20mol•L-1•s-1 |
 A的结构式如图,据你所学知识,判断A属于( )
A的结构式如图,据你所学知识,判断A属于( )| A. | 酸类 | B. | 醚类 | C. | 醛类 | D. | 酯类 |
| A. | $\frac{1}{6}$ | B. | $\frac{1}{4}$ | C. | $\frac{1}{3}$ | D. | $\frac{1}{2}$ |
| A. | 都增大 | B. | 都不变 | ||
| C. | 都减小 | D. | 有的增大,有的减小 |