题目内容
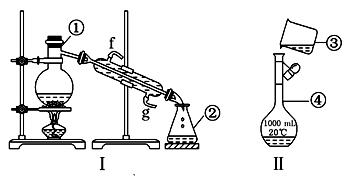
(13分)用下图装置可以进行测定SO2转化成SO3的转化率的实验。已知SO3的熔点是16.8℃,沸点是44.8℃。已知发生装置中所涉及反应的化学方程式为:
Na2SO3(s)+ H2SO4(85%)=Na2SO4 + SO2↑+ H2O

根据实验需要,应该在Ⅰ、Ⅱ、Ⅲ处连接合适的装置。请从下图A~E装置中选择最适合Ⅰ、Ⅱ、Ⅲ处连接的装置分别是 、 、 。
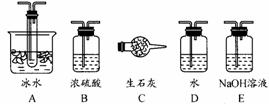
(2)从乙处均匀通入O2,为使SO2有较高的转化率,实验中在加热催化剂与滴加浓硫酸的顺序中,首先应采取的操作是 。
(3)有一小组在实验中发现,SO2气体产生缓慢,以致后续实验现象不明显,但又不存在气密性问题,请你推测可能的原因并说明相应的验证方法(写2点)。
①原因 ,验证方法
②原因 ,验证方法
(4)将SO2通入含1.5mol氯酸的溶液中,可生成一种强酸和一种氧化物,若有1.5×6.02×1023个电子转移时,该反应的化学方程式
(5)用amolNa2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,测得装置Ⅲ增重了bg,则实验中SO2的转化率为 %(用含a、b的代数式填写)
Na2SO3(s)+ H2SO4(85%)=Na2SO4 + SO2↑+ H2O

根据实验需要,应该在Ⅰ、Ⅱ、Ⅲ处连接合适的装置。请从下图A~E装置中选择最适合Ⅰ、Ⅱ、Ⅲ处连接的装置分别是 、 、 。

(2)从乙处均匀通入O2,为使SO2有较高的转化率,实验中在加热催化剂与滴加浓硫酸的顺序中,首先应采取的操作是 。
(3)有一小组在实验中发现,SO2气体产生缓慢,以致后续实验现象不明显,但又不存在气密性问题,请你推测可能的原因并说明相应的验证方法(写2点)。
①原因 ,验证方法
②原因 ,验证方法
(4)将SO2通入含1.5mol氯酸的溶液中,可生成一种强酸和一种氧化物,若有1.5×6.02×1023个电子转移时,该反应的化学方程式
(5)用amolNa2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,测得装置Ⅲ增重了bg,则实验中SO2的转化率为 %(用含a、b的代数式填写)
13分)(1) B A E(2分,错写1个扣1分,至0分,其它合理答案均给分)
(2)先加热催化剂再滴入浓硫酸(1分)
(3)①原因 Na2SO3变质(1分),
验证方法取待测试样于试管中,加适量蒸馏水配成溶液,先滴入足量稀盐酸,再滴入BaCl2溶液有白色沉淀生成,则证明该Na2SO3固体变质(2分)
②原因 不是浓硫酸 (1分),
验证方法用洁净玻璃棒蘸取待测试样,涂白纸不变黑,则证明该溶液不是浓硫酸(2分)(其他答案合理也给分)
(4)SO2 + 2HClO3 = H2SO4 + 2ClO2(2分)
(5)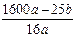 %(或者
%(或者 %)(2分)
%)(2分)
(2)先加热催化剂再滴入浓硫酸(1分)
(3)①原因 Na2SO3变质(1分),
验证方法取待测试样于试管中,加适量蒸馏水配成溶液,先滴入足量稀盐酸,再滴入BaCl2溶液有白色沉淀生成,则证明该Na2SO3固体变质(2分)
②原因 不是浓硫酸 (1分),
验证方法用洁净玻璃棒蘸取待测试样,涂白纸不变黑,则证明该溶液不是浓硫酸(2分)(其他答案合理也给分)
(4)SO2 + 2HClO3 = H2SO4 + 2ClO2(2分)
(5)
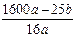 %(或者
%(或者 %)(2分)
%)(2分)略

练习册系列答案
相关题目
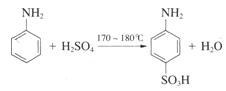

 胺及几粒沸石,
胺及几粒沸石,