题目内容
等体积、等物质的量浓度的NaCl和NaF溶液中,阴阳离子总数相比 ( )
| A.前者多 | B.后者多 | C.一样多 | D.无法判断 |
B
正确答案:B
NaF是强碱弱酸盐,F++H2O
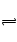 HF+OH― ,促进水电离。后者生成的OH―多,阴阳离子总数相比后者多。
HF+OH― ,促进水电离。后者生成的OH―多,阴阳离子总数相比后者多。
练习册系列答案
相关题目
题目内容
| A.前者多 | B.后者多 | C.一样多 | D.无法判断 |
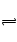 HF+OH― ,促进水电离。后者生成的OH―多,阴阳离子总数相比后者多。
HF+OH― ,促进水电离。后者生成的OH―多,阴阳离子总数相比后者多。