题目内容
17. 第四周期过渡元素Mn、Fe、Ti可与C、H、O形成多种化合物.
第四周期过渡元素Mn、Fe、Ti可与C、H、O形成多种化合物.(1)下列叙述正确的是A D.(填字母)
A.CH2O与水分子间能形成氢键
B.CH2O和CO2分子中的中心原子均采用sp2杂化
C.C6H6分子中含有6个σ键和1个大π键,C6H6是非极性分子
D.CO2晶体的熔点、沸点都比二氧化硅晶体的低
(2)Mn和Fe的部分电离能数据如下表:
| 元素 | Mn | Fe | |
| 电离能/kJ•mol-1 | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
(3)根据元素原子的外围电子排布的特征,可将元素周期表分成五个区域,其中Ti属于d区.
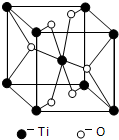
(4)Ti的一种氧化物X,其晶胞结构如图所示,则X的化学式为TiO2.
(5)电镀厂排放的废水中常含有剧毒的CN-离子,可在X的催化下,先用NaClO将CN-氧化成CNO-,再在酸性条件下CNO-继续被NaClO氧化成N2和CO2.
①H、C、N、O四种元素的电负性由小到大的顺序为H<C<N<O.
②与CNO-互为等电子体微粒的化学式为CO2(N2O)、SCN-(写出一种即可).
③氰酸(HOCN)是一种链状分子,它与异氰酸(HNCO)互为同分异构体,其分子内各原子最外层均已达到稳定结构,试写出氰酸的结构式N≡C-O-H.
分析 (1)A.甲醛中氧元素电负性很大,与水分子中H原子可以形成氢键;
B.CH2O分子中C原子形成3个σ键,而CO2分子中C原子形成2个σ键,均没有孤电子对;
C.C6H6分子中含有12个σ键和1个大π键;
D.二氧化碳晶体属于分子晶体,二氧化硅属于原子晶体.
(2)d电子半充满比较稳定,锰价电子排布为3d54s2,Mn2+转化为Mn3+时,3d能级由较稳定的3d5半充满状态转变为不稳定的3d4状态,而铁价电子排布为3d64s2,Fe2+转化为Fe3+时,3d能级由不稳定的3d6状态转变为较稳定的3d5半充满状态,气态Mn2+失去一个电子比气态Fe2+失去一个电子难;
(3)元素周期表根据元素原子的外围电子排布的特征分成五个区域,s区、p区、d区、ds区、f区,s区为第ⅠA、ⅡA族,p区为第ⅢA到零族,d区包括从第ⅢB族到八族,ds区为第ⅠB、ⅡB族,f区为镧系和锕系;
(4)晶胞中原子个数的计算,每个晶胞中含有钛原子数为2,氧原子数为4,可确定化学式为TiO2;
(5)①同周期从左向右,电负性逐渐增大,故电负性大小可以判断;
②等电子体为电子数相等,CNO-电子数为22,故与CNO-互为等电子体微粒的化学式CO2、N2O、SCN-等;
③碳为四配位,氮为三配位,氧为两配位,氰酸(HOCN)是一种链状分子,且其分子内各原子最外层均已达到稳定结构,故N≡C-O-H.
解答 解:(1)A.甲醛中氧元素电负性很大,与水分子中H原子可以形成氢键,故A正确;
B.CH2O分子中C原子形成3个σ键,而CO2分子中C原子形成2个σ键,均没有孤电子对,HCHO分子中C原子采用sp2杂化,二氧化碳分子中C原子为sp杂化,故B错误;
C.C6H6分子中含有12个σ键和1个大π键,故C错误;
D.二氧化碳晶体是分子晶体,二氧化硅晶体是原子晶体,所以CO2晶体的熔点、沸点都比二氧化硅晶体的低,故D正确,
故答案为:AD;
(2)25号元素锰,价电子个数为25-18=7,价电子排布为3d54s2,Mn2+转化为Mn3+时,3d能级由较稳定的3d5半充满状态转变为不稳定的3d4状态,而铁为26号元素,价电子排布为3d64s2,Fe2+转化为Fe3+时,3d能级由不稳定的3d6状态转变为较稳定的3d5半充满状态,故气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难;
故答案为:3d54s2; Mn2+转化为Mn3+时,3d能级由较稳定的3d5半充满状态转σσ变为不稳定的3d4状态,而Fe2+转化为Fe3+时,3d能级由不稳定的3d6状态转变为较稳定的3d5半充满状态;
(3)根据元素原子的外围电子排布的特征,可将元素周期表分成五个区域,s区、d区、ds区、p区、f区,s区为第ⅠA、ⅡA族,p区为第ⅢA到零族,d区包括从第ⅢB族到八族,ds区为第ⅠB、ⅡB族,f区为镧系和锕系,其中钛位于第ⅣB族,属于d区;
故答案为:d;
(4)每个晶胞中含有钛原子数为8×0.125+1=2,氧原子数为4×0.5+2=4,故化学式为TiO2;
故答案为:TiO2;
(5)①氢位于第一周期,碳、氮、氧元素位于第二周期,同周期从左向右,电负性逐渐增大,故电负性大小为H<C<N<O,
故答案为:H<C<N<O;
②CNO-电子数为22,等电子体为电子数相等,故与CNO-互为等电子体微粒的化学式CO2、N2O、SCN-等,
故答案为:CO2(N2O)、SCN-;
③氰酸(HOCN)是一种链状分子,且其分子内各原子最外层均已达到稳定结构,碳为四配位,氮为三配位,氧为两配位,故N≡C-O-H;
故答案为:N≡C-O-H.
点评 本题考查了物质结构和性质,涉及氢键、电负性、元素周期律、等电子体等知识点,知识点较综合,这些知识点都是考试热点,根据教材中基础知识采用知识迁移的方法进行分析解答,注意:元素周期表分成五个区域,s区、p区、d区、ds区、f区,s区为第ⅠA、ⅡA族,p区为第ⅢA到零族,d区包括从第ⅢB族到八族,ds区为第ⅠB、ⅡB族,f区为镧系和锕系,题目难度中等.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| Na | Cu | Al | Fe | |
| 熔点(℃) | 97.5 | 1083 | 660 | 1535 |
| 沸点(℃) | 883 | 2595 | 2200 | 3000 |
| A. | Cu和Al | B. | Fe和Cu | C. | Fe和Na | D. | Al和Na |
 决定物质性质的重要因素是物质的结构.请回答下列问题:
决定物质性质的重要因素是物质的结构.请回答下列问题:(1)已知A和B为第三周期元素,其原子的第一至第四电离如下表所示:
| 电离能/kJ•mol-1 | I1 | I2 | I3 | I4 |
| A | 578 | 1 817 | 2 745 | 11 578 |
| B | 738 | 1 451 | 7 733 | 10 540 |
(2)已知:波长为300nm的紫外光的光子所具有的能量约为399kJ•mol-1.根据下表有关蛋白质分子中重要化学键的信息,说明人体长时间照射紫外光后皮肤易受伤害的原因:紫外光具有的能量比蛋白质分子中重要的化学键C-C、C-N和C-S的键能都大,紫外光的能量足以使这些化学键断裂,从而破坏蛋白质分.
| 共价键 | C-C | C-N | C-S |
| 键能/kJ•mol-1 | 347 | 305 | 259 |
(4)某配合物的分子结构如图所示,其分子内不含有AC(填字母).
A.离子键 B.共价键 C.金属键 D.配位键 E.氢键.
| 用途 | 解释 | |
| A | 氨常用作制冷剂 | 液氨汽化时要吸收大量的热,使周围温度降低 |
| B | SO2 可用于漂白纸浆 | SO2 具有氧化性 |
| C | 明矾可用于净水 | 明矾在水中生成的氢氧化铝胶状物质,有吸附性 |
| D | 常温下,可用铁、铝制容器盛装浓硝酸 | 铁、铝表面被氧化成的致密氧化物薄膜,阻止了酸与内层金属的进一步反应 |
| A. | A | B. | B | C. | C | D. | D |
 已知:①N2(g)+O2(g)═2NO(g)△H1=+180kJ•mol-1
已知:①N2(g)+O2(g)═2NO(g)△H1=+180kJ•mol-1②N2(g)+3H2(g)?2NH3(g)△H2=-92.4kJ•mol-1
③2H2(g)+O2(g)═2H2O(g)△H3=-483.6kJ•mol-1
下列说法正确的是( )
| A. | 反应②中的能量变化如图所示,则△H2=E1-E3 | |
| B. | H2的燃烧热为241.8 kJ•mol-1 | |
| C. | 由反应②知在温度一定的条件下,在一恒容密闭容器中通入1mol N2和3mol H2,反应后放出的热量为Q1 kJ,若通入2mol N2和6mol H2反应后放出的热量为Q2 kJ,则184.8>Q2>2Q1 | |
| D. | 氨的催化氧化反应为4NH3(g)+5O2(g)═4NO(g)+6H2O(g)△H=+906 kJ•mol-1 |
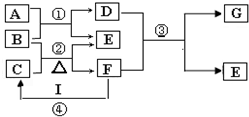
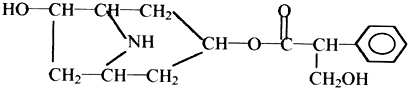
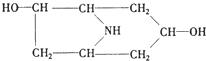 、C:
、C: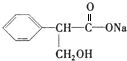 . 该反应属于水解反应;
. 该反应属于水解反应;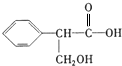 ;
;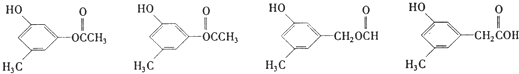 任意两种.
任意两种.