��Ŀ����
4������������Ҫ�ɷ���Al2O3����SiO2��Fe2O3��MgO�����ʣ�����ȡ�����������ֹ����������£�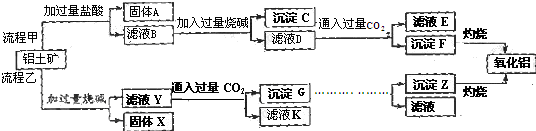
��ش��������⣺
��1��Fe��ԭ������Ϊ26��Feλ��Ԫ�����ڱ��е������ڣ���VIII�壮
��2�����̼������������Al3+�����ӷ���ʽΪAl2O3+6H+�T2Al3++3H2O��
��3�������Ҽ����ռ������SiO32-�����ӷ���ʽΪSiO2+2OH-�TSiO32-+H2O��
��4��д��������ҺB���Ƿ������ӵķ���ȡ��ҺB�������Թ��У����Թ��еμ�2��KSCN��Һ������Һ��Ϊ��ɫ˵����Һ�к���Fe3+���������Ա仯����Fe3+��
��5����ҺE��K�����ʵ���Ҫ�ɷ���NaHCO3���ѧʽ����д������Һ��һ����;�ƴ���������ͷ۵ȣ�
��6����֪298Kʱ��Mg��OH��2���ܶȻ�����Ksp=5.6��10-12��ȡ��������ҺB������һ�������ռ�ﵽ������Һƽ�⣬���pH=13.00������¶��²�������Һ�е�c��Mg2+��=5.6��10-10mol/L��
���� ��������Ҫ�ɷ���Al2O3����SiO2��Fe2O3��MgO�����ʣ��м���ϡ���ᣬAl2O3��Fe2O3��MgO�ֱ��ϡ���ᷴӦ����AlCl3��FeCl3��MgCl2��SiO2������ϡ���ᣬȻ����˵õ���AΪSiO2������ҺB�м�������ռAlCl3��FeCl3��MgCl2�ֱ��NaOH��Ӧ���ɿ����Ե�DΪNaAlO2�ͳ���CΪFe��OH��3��Mg��OH��2��Ȼ���ٹ��ˣ�����Һ��ͨ�����������̼������Al��OH��3����ͬʱ���ɿ�����NaHCO3���ٹ��ˣ���ҺE�����ʳɷ���NaHCO3������F��Al��OH��3��������F���յõ���������
�������м������NaOH��Һ��Al2O3��SiO2�����������Ʒֱ�õ������Ե�NaAlO2��Na2SiO3��Fe2O3��MgO������NaOH��Һ��Ȼ����˵õ�����XΪFe2O3��MgO����ҺY�к���NaOH��NaAlO2��Na2SiO3������Һ��ͨ�����������̼���õ�����GΪAl��OH��3��H2SiO3����Һ��KΪNaHCO3���������������õ�������������ZΪAl��OH��3���ݴ˴��⣮
��� �⣺��������Ҫ�ɷ���Al2O3����SiO2��Fe2O3��MgO�����ʣ��м���ϡ���ᣬAl2O3��Fe2O3��MgO�ֱ��ϡ���ᷴӦ����AlCl3��FeCl3��MgCl2��SiO2������ϡ���ᣬȻ����˵õ���AΪSiO2������ҺB�м�������ռAlCl3��FeCl3��MgCl2�ֱ��NaOH��Ӧ���ɿ����Ե�DΪNaAlO2�ͳ���CΪFe��OH��3��Mg��OH��2��Ȼ���ٹ��ˣ�����Һ��ͨ�����������̼������Al��OH��3����ͬʱ���ɿ�����NaHCO3���ٹ��ˣ���ҺE�����ʳɷ���NaHCO3������F��Al��OH��3��������F���յõ���������
�������м������NaOH��Һ��Al2O3��SiO2�����������Ʒֱ�õ������Ե�NaAlO2��Na2SiO3��Fe2O3��MgO������NaOH��Һ��Ȼ����˵õ�����XΪFe2O3��MgO����ҺY�к���NaOH��NaAlO2��Na2SiO3������Һ��ͨ�����������̼���õ�����GΪAl��OH��3��H2SiO3����Һ��KΪNaHCO3���������������õ�������������ZΪAl��OH��3��
��1��Fe��ԭ������Ϊ26��Feλ��Ԫ�����ڱ��е������ڣ���VIII �壬
�ʴ�Ϊ���ģ�VIII��
��2��Al2O3�����ᷴӦ�����Ȼ�����ˮ�������ﲻ�ܲ����ӷ���ʽΪ��Al2O3+6H+�T2Al3++3H2O��
�ʴ�Ϊ��Al2O3+6H+�T2Al3++3H2O��
��3�������������������Ʒ�Ӧ���ɹ����ƺ�ˮ���������費�ܲ𣬹����ӷ�Ӧ����ʽΪ��SiO2+2OH-�TSiO32-+H2O��
�ʴ�Ϊ��SiO2+2OH-�TSiO32-+H2O��
��4�������Ӻ�KSCN��Һ��Ӧ������������軯������Һ��Ѫ��ɫ������鷽��Ϊȡ��ҺB�������Թ��У����Թ��еμ�2��KSCN��Һ������Һ��Ϊ��ɫ˵����Һ�к���Fe3+���������Ա仯����Fe3+��
�ʴ�Ϊ��ȡ��ҺB�������Թ��У����Թ��еμ�2��KSCN��Һ������Һ��Ϊ��ɫ˵����Һ�к���Fe3+���������Ա仯����Fe3+��
��4��ͨ�����Ϸ���֪��E��K����ͬ����ΪNaHCO3��̼��������Һ��һ����;Ϊ �ƴ���������ͷ۵ȣ�
�ʴ�Ϊ��NaHCO3�� �ƴ���������ͷ۵ȣ�
��5����֪��ҺB�м���һ������NaOH�ﵽ������Һƽ��ʱpH=13.00����c��H+��=1��10-13mol/L��c��OH-��=$\frac{1��1{0}^{-14}}{1��1{0}^{-13}}$=0.1mol/L��
Mg��OH��2���ݶȻ�����KSP=c��Mg2+��•c2��OH-��=5.6��10-12��c��Mg2+��=$\frac{5.6��1{0}^{-12}}{0��{1}^{2}}$=5.6��10-10mol/L��
�ʴ�Ϊ��5.6��10-10mol/L��
���� ���⿼�����ʵķ�����ᴿ��Ϊ��Ƶ���㣬���ؿ���ѧ�������ƶϡ�֪ʶǨ����������ȷԪ�ػ����������ǽⱾ��ؼ���֪������ͼ�з����ķ�Ӧ������������ע��������п�����ڰ�ˮ����Ŀ�ѶȲ���

 ���źþ���Ԫ����ĩ��ϵ�д�
���źþ���Ԫ����ĩ��ϵ�д�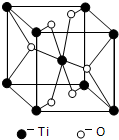 �������ڹ���Ԫ��Mn��Fe��Ti����C��H��O�γɶ��ֻ����
�������ڹ���Ԫ��Mn��Fe��Ti����C��H��O�γɶ��ֻ������1������������ȷ����A D��������ĸ��
A��CH2O��ˮ���Ӽ����γ����
B��CH2O��CO2�����е�����ԭ�Ӿ�����sp2�ӻ�
C��C6H6�����к���6���Ҽ���1����м���C6H6�ǷǼ��Է���
D��CO2������۵㡢�е㶼�ȶ������辧��ĵ�
��2��Mn��Fe�IJ��ֵ������������±���
| Ԫ�� | Mn | Fe | |
| ������/kJ•mol-1 | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
��3������Ԫ��ԭ�ӵ���Χ�����Ų����������ɽ�Ԫ�����ڱ��ֳ������������Ti����d����
��4��Ti��һ��������X���侧���ṹ��ͼ��ʾ����X�Ļ�ѧʽΪTiO2��
��5����Ƴ��ŷŵķ�ˮ�г����о綾��CN-���ӣ�����X�Ĵ��£�����NaClO��CN-������CNO-����������������CNO-������NaClO������N2��CO2��
��H��C��N��O����Ԫ�صĵ縺����С�����˳��ΪH��C��N��O��
����CNO-��Ϊ�ȵ��������Ļ�ѧʽΪCO2��N2O����SCN-��д��һ�ּ��ɣ���
�����ᣨHOCN����һ����״���ӣ����������ᣨHNCO����Ϊͬ���칹�壬������ڸ�ԭ���������Ѵﵽ�ȶ��ṹ����д������ĽṹʽN��C-O-H��
CO��g��+H2O��g���TCO2��g��+H2��g����H=-41kJ/molijС���о�����ͬ�¶��¸÷�Ӧ�����е������仯�����Ƿֱ��������ΪV L���������º����ܱ������м���һ�����ķ�Ӧ�ʹ������ͬ�¶��·�����Ӧ������������£�
| ������� | ��ʼʱ���������ʵ���/mol | �ﵽƽ���ʱ��/min | ��ƽ��ʱ��ϵ�����ı仯/kJ | ||||
| CO | H2O | CO2 | H2 | ||||
| �� | 1 | 4 | 0 | 0 | t1 | �ų�������32.8 kJ | |
| �� | 2 | 8 | 0 | 0 | t2 | �ų�������Q | |
��2���������з�Ӧ��ƽ��ʱ��CO��ת����Ϊ80%��
��3�������������з�Ӧ��ƽ�ⳣ��K=1��
��4������������ȷ����a������ĸ��ţ���
a��ƽ��ʱ����������H2������������
b���������з�Ӧ��ƽ��״̬ʱ��Q��65.6kJ
c����Ӧ��ʼʱ���������з�Ӧ�Ļ�ѧ��Ӧ�������
d���������У���ѧ��Ӧ����Ϊ��v��H2O��=$\frac{4}{V{t}_{1}}$mol/��L-min��
��5����֪��2H2��g��+O2��g��=2H2O ��g����H=-484kJ/mol��д��CO��ȫȼ������CO2���Ȼ�ѧ����ʽ2CO��g��+O2��g���T2CO2��g����H=-566kJ/mol
��6���������з�Ӧ���е�t minʱ����û��������CO2�����ʵ���Ϊ0.6mol������200mL 5mol/L��NaOH��Һ������ȫ���գ���Ӧ�����ӷ���ʽΪ����һ�����ӷ���ʽ��ʾ��3CO2+5OH-�T2CO32-+HCO3-+2H2O��
| A�� | �Ʊ�Fe��OH��3���壺Fe3++3OH-=Fe��OH��3�� | |
| B�� | ϡ�����м�����������ۣ�3Fe+2NO${\;}_{3}^{-}$+8H+=3Fe2++2NO��+4H2O | |
| C�� | ��Na2SiO3��Һ�м���ͨ�������H2S��SiO32-+H2SiO3��+S2- | |
| D�� | ��amolFel2��ˮ��Һ��ͨ��amol��Cl2��ӦΪ��2Fe2-+2l-+2Cl2=2Fe2++4Cl-+l2 |
| A�� | 2��3-���һ����� | B�� | 5-��-3-�һ����� | ||
| C�� | 2-��-4-�һ����� | D�� | 2��3��3-�������� |
| A�� | ��28 g����ϩ��֬�У����е�̼ԭ����ĿΪ2NA | |
| B�� | �ںϳ�28 g����ϩ��֬�ĵ����У����е�˫����ĿΪNA | |
| C�� | 28 g����ϩ��֬��ȫȼ��ʱ��ת�Ƶĵ�����ĿΪ3NA | |
| D�� | 28 g����ϩ��֬�У����е�C-H������ĿΪ4NA |
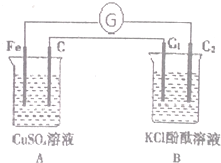 ��ͼװ�ý�������ʱ���۲쵽����ָ�뷢��ƫת��B����C2������Һ��죬�ش��������⣨C��C1��C2��Ϊʯī�缫��
��ͼװ�ý�������ʱ���۲쵽����ָ�뷢��ƫת��B����C2������Һ��죬�ش��������⣨C��C1��C2��Ϊʯī�缫��