题目内容
【题目】(1)常温下常压下,1g固态碳与水蒸气恰好完全反应,反应生成气体CO和H2,吸收10.94kJ热量,此反应的热化学方程式为___。
(2)已知:①CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH1=-Q1kJ·mol-1,
②2H2(g)+O2(g)=2H2O(g) ΔH2=-Q2kJ·mol-1,
③2H2(g)+O2(g)=2H2O(l) ΔH3=-Q3kJ·mol-1。
常温下,取体积比4∶1的甲烷和氢气的混合气体11.2L(标准状况下),经完全燃烧后恢复至室温,则放出的热量为___kJ。
(3)以H2为燃料可制成氢氧燃料电池。已知:2H2(g)+O2(g)=2H2O(l) ΔH=-572kJ·mol-1,某氢氧燃料电池释放228.8kJ电能时,生成1mol液态水,该电池的能量转化率为___。
【答案】C(s)+H2O(g)═CO(g)+H2(g) △H=+131.28kJmol-1; 0.4Q1+0.05Q3 80%
【解析】
(1)由1g碳与适量水蒸气反应生成CO和H2,需吸收10.94kJ热量,则1mol碳与水蒸气反应,吸收10.94KJ×12=131.28kJ,并注意物质的状态来解答;
(2)根据混合气体的体积计算混合气体的物质的量,结合气体体积比计算甲烷、氢气的物质的量,再根据热化学反应方程式计算放出的热量,注意燃烧后恢复至常温,氢气燃烧放出的热量应选择生成液态水的热化学反应方程式计算;
(3)先根据热化学方程式求出生成1mol液态水,理论上放出的能量,然后根据电池的能量转化率=![]() ×100%。
×100%。
(1)由1g碳与适量水蒸气反应生成CO和H2,需吸收10.94kJ热量,则1mol碳与水蒸气反应,吸收10.94KJ×12=131.28kJ,则此反应的热化学方程式为C(s)+H2O(g)═CO(g)+H2(g) △H=+131.28kJmol-1,故答案为:C(s)+H2O(g)═CO(g)+H2(g) △H=+131.28kJmol-1;
(2)甲烷和氢气的混合气体11.2L(已折合成标准状况),所以甲烷和氢气的混合气体的总的物质的量为=![]() =0.5mol,甲烷和氢气的体积比为4:1,所以甲烷的物质的量为0.5mol×
=0.5mol,甲烷和氢气的体积比为4:1,所以甲烷的物质的量为0.5mol×![]() =0.4mol,氢气的物质的量为0.5mol-0.4mol=0.1mol,由CH4(g)+2O2(g)═CO2(g)+2H2O(l) △H=-Q1kJ/mol可知,0.4mol甲烷燃烧放出的热量为0.4mol×Q1kJ/mol=0.4Q1kJ;由2H2(g)+O2(g)═2H2O(l) △H=-Q3kJ/mol可知,0.1mol氢气燃烧生成液态水放出的热量为0.1mol×
=0.4mol,氢气的物质的量为0.5mol-0.4mol=0.1mol,由CH4(g)+2O2(g)═CO2(g)+2H2O(l) △H=-Q1kJ/mol可知,0.4mol甲烷燃烧放出的热量为0.4mol×Q1kJ/mol=0.4Q1kJ;由2H2(g)+O2(g)═2H2O(l) △H=-Q3kJ/mol可知,0.1mol氢气燃烧生成液态水放出的热量为0.1mol×![]() ×Q3kJ/mol=0.05Q3kJ,所以放出的热量为(0.4Q1+0.05Q3)kJ,故答案为:0.4Q1+0.05Q3;
×Q3kJ/mol=0.05Q3kJ,所以放出的热量为(0.4Q1+0.05Q3)kJ,故答案为:0.4Q1+0.05Q3;
(3)生成1mol液态水,理论上放出的能量为![]() =286kJ,电池的能量转化率=
=286kJ,电池的能量转化率=![]() ×100%=
×100%=![]() ×100%=80%,故答案为:80%。
×100%=80%,故答案为:80%。

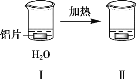
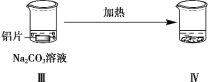
【题目】探究铝片与Na2CO3溶液的反应,下列说法不正确的是( )
|
| |
无明显现象 | 铝片表面产生细小气泡 | 出现白色浑浊,产生大量气泡(经检验为H2和CO2) |
A.对比Ⅰ、Ⅲ,说明Na2CO3溶液能破坏铝表面的保护膜
B.Na2CO3溶液中存在平衡:CO32-+H2O![]() HCO3- +OH-
HCO3- +OH-
C.加热和H2逸出对CO32-水解平衡移动方向的影响是相反的
D.推测出现白色浑浊的原因:AlO2-+HCO3-+H2O=Al(OH)3↓+CO32-