题目内容
【题目】有A、B两个完全相同的装置,某学生分别在它们的侧管中装入一定量的Na2CO3和NaHCO3,A、B中分别装有足量的盐酸,将两个侧管中的物质同时倒入各自的试管中,下列叙述正确的是
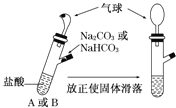
A. 侧管中装入Na2CO3的气球膨胀速率大
B. 若加入等质量的Na2CO3和NaHCO3 ,最终两气球体积不同
C. 最终两试管中Na+、Cl-的物质的量一定相同
D. 热稳定性:Na2CO3 < NaHCO3
【答案】B
【解析】A.碳酸钠和酸反应分步进行,先生成碳酸氢钠,后碳酸氢钠和盐酸反应生成二氧化碳,所以A装置的气球膨胀速率慢,故A错误;B.若加入等质量的Na2CO3和NaHCO3 ,则碳酸钠的物质的量小于碳酸氢钠,最终碳酸氢钠的气球体积大,故B正确;C.0.01molNa2CO3和0.01molNaHCO3的物质的量相等,所以Na2CO3和 NaHCO3中钠离子的物质的量不同,故最终两试管中Na+的物质的量一定不相同,故C错误;D.热稳定性:Na2CO3 > NaHCO3,故D错误;故选B。

练习册系列答案
 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案
相关题目