题目内容
【题目】Li-SO2充电电池具有高输出功率的优点。多孔碳电极可吸附SO2,电解液为溶解有LiBr的碳酸丙烯酯-乙腈溶液。下列说法错误的是( )
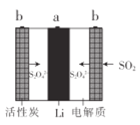
A.活性炭具有加快放电速率的作用
B.放电时,电子流向:a→溶液→b→a
C.充电时,阳极上发生的电极反应为:S2O42--2e-=2SO2
D.该电池的电解质溶液不能换成LiBr的水溶液
【答案】B
【解析】
Li为活泼金属,为负极,吸附了SO2的多孔碳电极为正极,结合原电池原理和电解池原理分析解答。
A.多孔活性炭电极的表面积大,增大了反应的接触面积,速率加快,故A正确;
B.高电池中a为负极,b为正极,原电池中电子不能经过电解质溶液,而是经过外电路,电子流向是a经用电器到b,故B错误;
C.充电时,电池的正极是电解池的阳极,电极反应是正极反应的逆过程,即S2O42--2e-═2SO2,故C正确;
D.活泼金属锂能够与电解质溶液中的水反应,则该电池的电解质溶液不能换成LiBr的水溶液,故D正确;
故选B。

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
