题目内容
用FeCl3溶液腐蚀印刷电路板上的铜,所得的溶液中加入铁粉。对加入铁粉充分反应后的溶液分析合理的是
| A.若无固体剩余,则溶液中一定有Fe3+ |
| B.若有固体存在,则溶液中一定有Fe2+ |
| C.若溶液中有Cu2+,则一定没有固体析出 |
| D.若溶液中有Fe2+,则一定有Cu析出 |
B
试题分析:氧化性是Fe3+>Cu2+>Fe2+,还原性是Fe>Cu,则A、若无固体剩余,这说明铁粉完全被溶液中的铁离子氧化,但此时溶液中不一定还有Fe3+,A不正确;B、若有固体存在,则固体中一定有铜,可能还有铁,因此溶液中一定有Fe2+,B正确;C、若溶液中有Cu2+,则也可能有部分铜已经被置换出来,因此不一定没有固体析出,C不正确;D、若溶液中有Fe2+,但如果溶液铁离子过量,则不一定有Cu析出,D不正确,答案选B。

练习册系列答案
相关题目




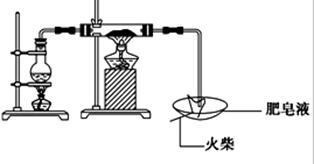
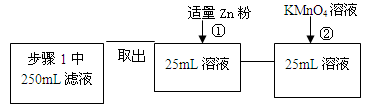
 下列说法正确的是
下列说法正确的是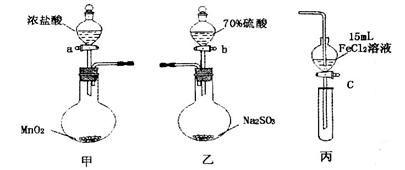

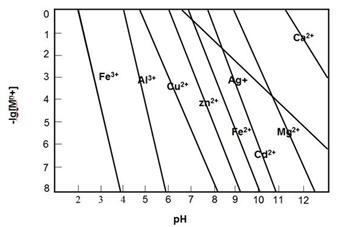
 R2Cu(有机相)+2H+(水相),已知其它阳离子与该有机物不能发生反应,也不相溶。请设计实验方案,验证有机相中含有铜元素。
R2Cu(有机相)+2H+(水相),已知其它阳离子与该有机物不能发生反应,也不相溶。请设计实验方案,验证有机相中含有铜元素。