题目内容
【题目】下列电离方程式书写不正确的是
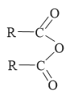
A.HNO3=H+ + NO![]() B.Al2(SO4)3=2Al3+ + 3SO
B.Al2(SO4)3=2Al3+ + 3SO![]()
C.Ba(OH)2=Ba2+ + 2OH-D.NaHCO3=Na+ + H+ + CO![]()
【答案】D
【解析】
A.HNO3为强电解质,能完全电离,电离方程式为HNO3=H+ + NO![]() ,遵循质量守恒定律和电荷守恒,A正确;
,遵循质量守恒定律和电荷守恒,A正确;
B.Al2(SO4)3为强电解质,能完全电离,电离方程式为Al2(SO4)3=2Al3+ + 3SO![]() ,遵循质量守恒定律和电荷守恒,B正确;
,遵循质量守恒定律和电荷守恒,B正确;
C.Ba(OH)2为强电解质,能完全电离,电离方程式为Ba(OH)2=Ba2+ + 2OH-,遵循质量守恒定律和电荷守恒,C正确;
D.NaHCO3为强电解质,第一步完全电离,电离方程式为NaHCO3=Na+ + HCO3-,第二步部分电离,电离方程式为HCO3-![]() H+ + CO
H+ + CO![]() ,D错误;
,D错误;
故选D。

 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案 导学与测试系列答案
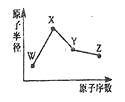
导学与测试系列答案【题目】A、B、C、D、E是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如下:
元素 | 相关信息 |
A | 基态原子的价电子排布式为nSnnPn |
B | 基态原子中的未成对电子数是同周期中最多的 |
C | 最外层电子数是电子层数的3倍 |
D | 简单离子是第三周期元素中离子半径最小的 |
E | 价电子层中的未成对电子数为4 |
请回答下列问题(用对应元素的元素符号作答):
(1)写出D元素基态原子的价电子排布式_________,E2+价电子的轨道表示式_________________。
(2)这5种元素中电负性最大的元素是_____(填元素符号),A、B、C三种元素的第一电离能由大到小的顺序为_______________(填元素符号)
(3)B、C、D的简单离子的半径由大到小的顺序为_____________(用离子符号表示)
(4)写出C的核外有18个电子的氢化物的电子式_____________。
【题目】下列实验过程中对应的变化与右图相符合的是
实验过程 | X | Y |
| |
A | 稀HCl滴加到NaOH溶液中 | V(HCl) | N(Na+) | |
B | 铁粉加入 CuSO4溶液中 | m(Fe) | m(固 体) | |
C | CO2通入NaOH溶液中 | V(CO2) | 溶液的导电能力 | |
D | 稀H2SO4滴加到 Ba(OH)2溶液中 | V(H2SO4) | 溶液的导电能力 |
A. A B. B C. C D. D
【题目】用H2O2、KI和洗洁精可完成“大象牙膏”实验(短时间内产生大量泡沫),某同学依据文献资料对该实验进行探究。
(1)资料1:KI在该反应中的作用:
H2O2+I-=H2O+IO-;H2O2+IO-=H2O+O2↑+I-。总反应的化学方程式是________________。
(2)资料2:H2O2分解反应过程中能量变化如图所示,其中①有KI加入,②无KI加入。下列判断正确的是___________(填字母)。
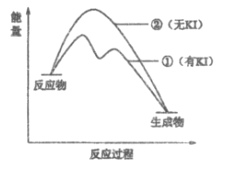
a. 加入KI后改变了反应的路径
b. 加入KI后改变了总反应的能量变化
c. H2O2+I-=H2O+IO-是放热反应
(3)实验中发现,H2O2与KI溶液混合后,产生大量气泡,溶液颜色变黄。再加入CCl4,振荡、静置,气泡明显减少。
资料3:I2也可催化H2O2的分解反应。
①加CCl4并振荡、静置后还可观察到___________,说明有I2生成。
②气泡明显减少的原因可能是:i. H2O2浓度降低;ii. ________。以下对照实验说明i不是主要原因:向H2O2溶液中加入KI溶液,待溶液变黄后,分成两等份于A、B两试管中。A试管加入CCl4,B试管不加CCl4,分别振荡、静置。观察到的现象是_____________。
(4)资料4:I-(aq)+I2(aq)![]() I3-(aq) K=640。
I3-(aq) K=640。
为了探究体系中含碘微粒的存在形式,进行实验:向20 mL一定浓度的H2O2溶液中加入10mL 0.10mol·L-1 KI溶液,达平衡后,相关微粒浓度如下:
微粒 | I- | I2 | I3- |
浓度/(mol·L-1) | 2.5×10-3 | a | 4.0×10-3 |
①a=__________。
②该平衡体系中除了含有I-,I2,I3-外,一定还含有其他含碘微粒,理由是________________。