题目内容
10.下列物质之间的转化,不能一步实现的是( )| A. | Na2O→NaOH | B. | NaHCO3→Na2CO3 | C. | SiO2→H2SiO3 | D. | NH3→NO |
分析 A.Na2O可与水反应生成NaOH;
B.NaHCO3与NaOH反应生成Na2CO3;
C.SiO2与水不反应;
D.NH3催化氧化生成NO.
解答 解:A.Na2O为碱性氧化物,可与水反应生成NaOH,故A正确;
B.NaHCO3与NaOH反应生成Na2CO3,同时生成水,故B正确;
C.SiO2与水不反应,应先与氢氧化钠反应,然后再与酸反应,故C错误;
D.NH3催化氧化生成NO,故D正确.
故选C.
点评 本题考查物质的转化,要熟练掌握元素及其化合物之间的转化关系,具有一定的难度,尤其是不能一步转化的反应要注意.

练习册系列答案
相关题目
20.以NA表示阿佛加德罗常数,下列说法正确的是( )
| A. | 32gO2和32gO3的质子数均为16NA | |
| B. | 23gNa与O2在加热条件充分反应,O2得到的电子数为2NA | |
| C. | 在标准状况下,22.4LSO3所含分子数为NA | |
| D. | 2 L1mol•L-1的HC1溶液中,含有的HC1分子数目为2NA |
1.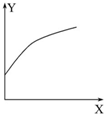 在密闭的容积可变的容器中通入A、B两种气体,在一定条件下反应:2A(g)+B(g)?2C(g)△H<0.达到平衡后,改变一个条件,下列量(Y)的变化不符合图中曲线的是( )
在密闭的容积可变的容器中通入A、B两种气体,在一定条件下反应:2A(g)+B(g)?2C(g)△H<0.达到平衡后,改变一个条件,下列量(Y)的变化不符合图中曲线的是( )
 在密闭的容积可变的容器中通入A、B两种气体,在一定条件下反应:2A(g)+B(g)?2C(g)△H<0.达到平衡后,改变一个条件,下列量(Y)的变化不符合图中曲线的是( )
在密闭的容积可变的容器中通入A、B两种气体,在一定条件下反应:2A(g)+B(g)?2C(g)△H<0.达到平衡后,改变一个条件,下列量(Y)的变化不符合图中曲线的是( )| X | Y | |
| A | 再加入A | B的转化率 |
| B | 降低温度 | 混合气体的密度 |
| C | 增大压强 | A的转化率 |
| D | 升高温度 | 混合气体的平均摩尔质量 |
| A. | A | B. | B | C. | C | D. | D |
18.碱性电池具有容量大、放电电流大的特点,因而得到广泛应用.锌-锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn(s)+2MnO2(s)+H2O(l)═Zn(OH)2(s)+Mn2O3(s).则下列说法正确的是( )
| A. | .电池工作时,MnO2发生还原反应 | |
| B. | .电池负极的电极反应式为:2MnO2+H2O+2e-→Mn2O3+2OH- | |
| C. | .电池工作时,电路中每通过0.2mol电子,锌的质量理论上减少6.5g | |
| D. | 电池工作时,K+移向负极 |
15.设NA 表示阿伏加德罗常数的值.下列说法正确的是( )
| A. | 0.1 mol 甲基(-CH3)中含有的电子总数为NA | |
| B. | 标准状况下,11.2 L乙醇所含碳原子数目为NA | |
| C. | 常温常压下,26 g 苯中所含的碳碳双键数为NA | |
| D. | 23g钠在足量氧气充分燃烧,转移电子数为NA |
2.下列依据相关实验得出的结论正确的是( )
| A. | 向溴水中通入某气体,溴水颜色褪去,说明该气体一定是乙烯 | |
| B. | 向海鲜浸出液中加入新制氢氧化铜,加热,产生红色沉淀,说明浸出液中可能含甲醛 | |
| C. | 向溴乙烷中直接加入硝酸银溶液,无浅黄色沉淀生成,说明该溴乙烷已变质 | |
| D. | 向蛋清中滴加CuSO4溶液,有固体析出,加水固体不溶解,说明蛋白质发生变性 |
20.某市髙速公路发生苯酚槽罐车泄漏事故,导致部分苯酚泄漏并造成污染.下列对于苯酚的叙述中,错误的是( )
| A. | 对泄露的苯酚用石灰水中和比用酒精冲洗掉的方法好 | |
| B. | 其浓溶液对皮肤有强烈的腐蚀性,如果不慎沾在皮肤上,应立即用酒精擦洗 | |
| C. | 其在水中的溶解度随温度的升髙而增大,超过65℃可以与水以任意比互溶 | |
| D. | 碳酸氢钠溶液中滴人苯酚的水溶液后会放出二氧化碳 |
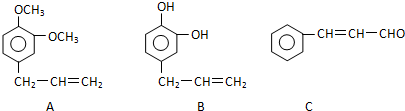
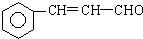 +5H2$\stackrel{一定条件下}{→}$
+5H2$\stackrel{一定条件下}{→}$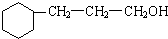 .
.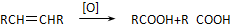 写出C在强氧化剂条件下生成的有机化合物的结构简式
写出C在强氧化剂条件下生成的有机化合物的结构简式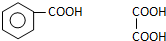 .
.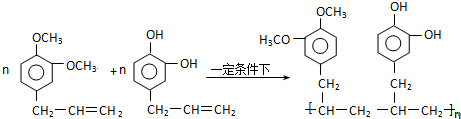 .
.