��Ŀ����
����Ŀ��̼��������Ԫ�ؼ��仯���������������������������ء�
I��̼�Ļ������ת���������������о�����Ҫ��Ӧ�á��ر���CO2�ĵ�̼ת�ͶԵ�������仯������Ҫ���塣
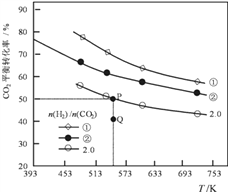
�������ݻ���Ϊ1L���ܱ��������Բ�ͬ����̼��n(H2)/n(CO2)����H2��CO2����һ�������·�����Ӧ��
2CO2(g) + 6H2(g) ![]() C2H4(g) + 4H2O(g) ��H��CO2��ƽ��ת�������¶ȵĹ�ϵ��ͼ��ʾ���١��ڡ�2.0�ֱ����������̼��ʱ�ı仯����)��
C2H4(g) + 4H2O(g) ��H��CO2��ƽ��ת�������¶ȵĹ�ϵ��ͼ��ʾ���١��ڡ�2.0�ֱ����������̼��ʱ�ı仯����)��
��ش��������⣺
��1����Ӧ�ġ�H_____0����̼����________�ڣ�Q��v(��)_____v(��)(����ڡ���С�ڡ�)
��2������ʼʱ��CO2��Ũ��Ϊ0.5mol/L��������Ũ��Ϊ1.0mol/L����P���Ӧ�¶ȵ�ƽ�ⳣ����ֵΪ_____________________��
II���ȵĻ�����ϳɡ�ת��һֱ�ǿ�ѧ�о����ȵ㡣
��һ�������£������백����Ӧ�����Ʊ��Ȱ�[NH2Cl(g)]����֪���ֻ�ѧ���ļ��ܣ�
��������Ӧ���Ȼ�ѧ����ʽΪ_______________________________________________________��
��ѧ�� | N��H | Cl��Cl | N��Cl | H��Cl |
����/kJ��mol-1 | 391.3 | 243.0 | 191.2 | 431.8 |
���Ȱ���һ�ֳ�Ч���ͺ������������л������־õ�ɱ�����ã�����ɱ��H7N9�����в�����������ԭ��Ϊ��ˮ������Ӧ����ǿ�����Ե����ʣ��÷�Ӧ�Ļ�ѧ����ʽΪ
_________________________________________________________��
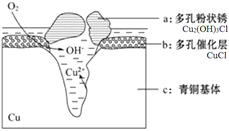
III���ð�ˮ��ȥSO2
(1)��֪25��ʱ��NH3��H2O��Kb=1.8��10-5��H2SO3��Ka1=1.3��10-2��Ka2=6.2��10-8.����ˮ��Ũ��Ϊ2.0mol/L������Һ�е�c(OH-)=_________mol/L.��SO2ͨ��ð�ˮ�У���c(OH-)����1.0��10-7mol/Lʱ����Һ�е�c(SO32-)/c(HSO3-)=_____________.
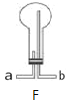
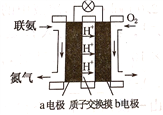
(2)���ð������������������ȡ����N2H4.��ͼ���ɡ�����-�������γɵ���ɫȼ�ϵ��,��ʯīΪ�缫�ĵ�ع���ԭ��ʾ��ͼ,b�缫Ϊ____________��(���������),д���õ�ع���ʱa�缫�ĵ缫��Ӧʽ___________________________________________.
���𰸡� С�� ���� ���� 512L3/mol3 NH3(g)+Cl2(g)=NH2Cl(g)+HCl(g) ��H=+11.3kJ/mol NH2Cl+H2O![]() NH3+HClO��NH2Cl+2H2O
NH3+HClO��NH2Cl+2H2O![]() NH3��H2O+HClO 6.0��10-3 0.62 �� N2H4-4e-=N2+4H+
NH3��H2O+HClO 6.0��10-3 0.62 �� N2H4-4e-=N2+4H+
��������������Ҫ���黯ѧ��Ӧԭ���ۺ����⡣
I����1��CO2��ƽ��ת���������¶����߶���С����������ƽ�����ƣ���Ӧ�ġ�HС��0������ͬ�¶��£�CO2��ƽ��ת��������������������̼���������ڣ���һ���¶�����Q��ﵽƽ������У�CO2��ת������������v(��)����v(��)��
��2��ƽ��ʱ��CO2��Ũ��Ϊ0.25mol/L��������Ũ��Ϊ0.25mol/L����ϩ��Ũ��Ϊ0.125mol/L��ˮ������Ũ��Ϊ0.5mol/L����P���Ӧ�¶ȵ�ƽ�ⳣ��Ϊ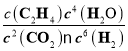 =512L3/mol3��
=512L3/mol3��
II������H=��Ӧ�����֮��-���������֮��=(3��391.3+243.0-191.2-2��391.3-431.8)kJ/mol=+11.3kJ/mol����������Ӧ���Ȼ�ѧ����ʽΪNH3(g)+Cl2(g)=NH2Cl(g)+HCl(g) ��H=+11.3kJ/mol��
���Ȱ���ˮ������Ӧ���ɵ�ǿ�����������Ǵ����ᣬ�÷�Ӧ�Ļ�ѧ����ʽΪNH2Cl+2H2O![]() NH3��H2O+HClO��
NH3��H2O+HClO��
III��(1)Kb=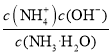 =1.8��10-5��c(NH3��H2O)=2.0mol/L����c(OH-)��c(NH4+)=
=1.8��10-5��c(NH3��H2O)=2.0mol/L����c(OH-)��c(NH4+)=![]() =6.0��10-3mol/L. Ka2��
=6.0��10-3mol/L. Ka2��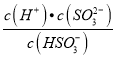 =6.2��10-8��c(H+)=c(OH-)=1.0��10-7mol/L����Һ�е�c(SO32-)/c(HSO3-)=Ka2/ c(H+)=0.62.
=6.2��10-8��c(H+)=c(OH-)=1.0��10-7mol/L����Һ�е�c(SO32-)/c(HSO3-)=Ka2/ c(H+)=0.62.
(2) O2��b�缫����ԭ������b�缫Ϊ�������õ�ع���ʱa�缫�ĵ缫��Ӧʽ��N2H4-4e-=N2+4H+.

����Ŀ����һ��������ܱ������У��������»�ѧ��Ӧ��CO2��g��+H2��g��CO��g��+H2O��g�����仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���
t�� | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
�ش��������⣺
��1���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪ��
��2����Ӧ����Ӧ����ѡ����ȡ������ȣ���
��3�����жϸ÷�Ӧ�Ƿ�ﵽ��ѧƽ��״̬�������� ��
a��������ѹǿ���� b�����������c��CO������
c��v����H2��=v����H2O�� d��c��CO2��=c��CO��
��4��ij�¶��£�ƽ��Ũ�ȷ�����ʽ��c��CO2��c��CH2��=c��CO��c��H2O�������жϴ�ʱ���¶�Ϊ��