题目内容
【题目】已知:NH2COO-+2H2O![]() HCO3-+NH3˙H2O。现用两份氨基甲酸铵溶液在不同温度(T1和T2)下实验,得到c(NH2COO-)随时间变化关系如图所示.以下分析正确的是
HCO3-+NH3˙H2O。现用两份氨基甲酸铵溶液在不同温度(T1和T2)下实验,得到c(NH2COO-)随时间变化关系如图所示.以下分析正确的是

A.无法判断T1和T2的大小关系
B.T1℃时,第6min反应物转化率为6.25%
C.T2℃时,0~6minν(NH2COO-)=0.3molL-1min-1
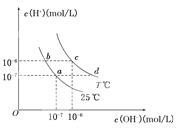
D.往平衡体系加水稀释,平衡右移,溶液中各种离子浓度减小
【答案】B
【解析】
试题分析:A.根据图可知,在6min时,T2的浓度变化了0.3molL-1,T1的浓度变化了0.15molL-1,而T2的起始浓度低于T1的,由此可知T2>T1,故A错误;B.根据转化率=![]() ×100%可知,T1℃时,第6min反应物转化率为
×100%可知,T1℃时,第6min反应物转化率为![]() ×100%=6.25%,故B正确;C.根据v=
×100%=6.25%,故B正确;C.根据v=![]() 可知,T2℃时,0~6minν(NH2COO-)=
可知,T2℃时,0~6minν(NH2COO-)=![]() molL-1min-1=0.05molL-1min-1,故C错误;D.往平衡体系加水稀释,温度不变,水的离子积常数不变,所以氢离子和氢氧根离子不可能同时减小或同时增大,故D错误;故选B。
molL-1min-1=0.05molL-1min-1,故C错误;D.往平衡体系加水稀释,温度不变,水的离子积常数不变,所以氢离子和氢氧根离子不可能同时减小或同时增大,故D错误;故选B。

练习册系列答案
相关题目
【题目】有些古文或谚语包含了丰富的化学知识。下列解释错误的是
选项 | 古文或谚语 | 化学解释 |
A | 日照香炉生紫烟 | 碘的升华 |
B | 以曾青涂铁,铁赤色如铜 | 置换反应 |
C | 煮豆燃豆萁 | 化学能转化为热能、光能 |
D | 雷雨肥庄稼 | 自然固氮 |
A.AB.BC.CD.D