题目内容
用中和滴定法测定烧碱的纯度,若烧碱中含有少量不与酸作用的可溶性杂质,试根据实验回答:(1)准确称取4.1g烧碱样品.
(2)将样品配成250mL待测液,需要的仪器有小烧杯、玻璃棒、______、胶头滴管.
(3)用______量取10mL待测液于______中(填仪器名称),并滴加几滴甲基橙作指示剂.
(4)用0.2010mol?L-1标准盐酸滴定待测烧碱溶液,滴定时______手旋转______式滴定管的玻璃活塞,______手不停地摇动锥形瓶,两眼注视锥形瓶内溶液颜色的变化,直到滴定终点,滴定终点时锥形瓶内溶液的PH约为______,达到终点的具体现象是:______.
(5)若两次实验滴定的数据如下表:
| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 10.00 | 0.50 | 20.4 |
| 第二次 | 10.00 | 4.00 | 24.1 |
(6)根据上述各数据,计算烧碱的纯度:______
(7)滴定时,滴定管尖嘴部分滴定前有气泡,滴定终了无气泡,测定结果将______(填偏高、偏低或无影响,其它操作均正确).
【答案】分析:(2)还需要250mL容量瓶;
(3)用碱式滴定管量取烧碱溶液与锥形瓶中;
(4)滴定时左手旋转酸式滴定管,右手不停地摇动锥形瓶;甲基橙的变色范围是3.1~4.4;滴定终点现象是:溶液由黄色变为橙色,且半分钟不变色;
(5)所耗盐酸标准液的体积分别为:19.90mL,20.10mL两组数据均有效,盐酸标准液的平均体积为20.00mL;带人公式c(待测)=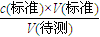 计算;
计算;
(6)根据m(烧碱)═C(烧碱)?V(烧碱溶液)?M(烧碱)求出烧碱质量,再计算出烧碱的质量分数;
(7)滴定管尖嘴部分滴定前有气泡,滴定终了无气泡,消耗的标准液体积偏大,浓度偏高.
解答:解:(2)将样品配成250mL待测液,需要250mL容量瓶,故答案为:250mL容量瓶;
(3)烧碱溶液需要用碱式滴定管量取,用锥形瓶盛放待测液,故答案为:碱式滴定管;锥形瓶;
(4)滴定时左手旋转酸式滴定管的玻璃活塞,右手不停地摇动锥形瓶,两眼注视锥形瓶内溶液颜色的变化;甲基橙的变色范围是:3.1~4.4;滴定终点现象是:溶液由黄色变为橙色,且半分钟不变色;
故答案为:左;酸; 右; 3.1~4.4;溶液由黄色变为橙色,且半分钟不变色;
(5)标准液的体积分别为:19.90mL,20.10mL,两组数据都有效,平均体积为20.00mL,带人公式可得:c(待测)=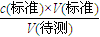 =
=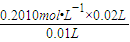 =0.4020 mol?L-1;
=0.4020 mol?L-1;
故答案为:0.4020 mol?L-1;
(6)m(烧碱)═C(烧碱)?V(烧碱溶液)?M(烧碱)═0.4020mol?L-1×0.25L×40g/mol=4.020g,烧碱的纯度ω(烧碱)=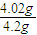 ×100%=98.05%;
×100%=98.05%;
故答案为:98.05%;
(7)滴定管尖嘴部分滴定前有气泡,滴定终了无气泡,消耗的标准液体积偏大,浓度偏高,故答案为:偏高.
点评:本题考查中和滴定,根据所学知识完成,涉及物质的量浓度计算、质量分数的计算,内容较多,难度稍大.
(3)用碱式滴定管量取烧碱溶液与锥形瓶中;
(4)滴定时左手旋转酸式滴定管,右手不停地摇动锥形瓶;甲基橙的变色范围是3.1~4.4;滴定终点现象是:溶液由黄色变为橙色,且半分钟不变色;
(5)所耗盐酸标准液的体积分别为:19.90mL,20.10mL两组数据均有效,盐酸标准液的平均体积为20.00mL;带人公式c(待测)=
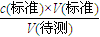 计算;
计算;(6)根据m(烧碱)═C(烧碱)?V(烧碱溶液)?M(烧碱)求出烧碱质量,再计算出烧碱的质量分数;
(7)滴定管尖嘴部分滴定前有气泡,滴定终了无气泡,消耗的标准液体积偏大,浓度偏高.
解答:解:(2)将样品配成250mL待测液,需要250mL容量瓶,故答案为:250mL容量瓶;
(3)烧碱溶液需要用碱式滴定管量取,用锥形瓶盛放待测液,故答案为:碱式滴定管;锥形瓶;
(4)滴定时左手旋转酸式滴定管的玻璃活塞,右手不停地摇动锥形瓶,两眼注视锥形瓶内溶液颜色的变化;甲基橙的变色范围是:3.1~4.4;滴定终点现象是:溶液由黄色变为橙色,且半分钟不变色;
故答案为:左;酸; 右; 3.1~4.4;溶液由黄色变为橙色,且半分钟不变色;
(5)标准液的体积分别为:19.90mL,20.10mL,两组数据都有效,平均体积为20.00mL,带人公式可得:c(待测)=
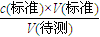 =
=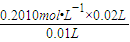 =0.4020 mol?L-1;
=0.4020 mol?L-1;故答案为:0.4020 mol?L-1;
(6)m(烧碱)═C(烧碱)?V(烧碱溶液)?M(烧碱)═0.4020mol?L-1×0.25L×40g/mol=4.020g,烧碱的纯度ω(烧碱)=
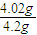 ×100%=98.05%;
×100%=98.05%;故答案为:98.05%;
(7)滴定管尖嘴部分滴定前有气泡,滴定终了无气泡,消耗的标准液体积偏大,浓度偏高,故答案为:偏高.
点评:本题考查中和滴定,根据所学知识完成,涉及物质的量浓度计算、质量分数的计算,内容较多,难度稍大.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目