��Ŀ����
���ԭ���ڻ�ѧ��ҵ���й㷺Ӧ�á���ͼ��ʾһ�����أ�װ�е��Һa��X��Y������缫�壬ͨ��������ֱ����Դ��������ش�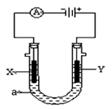
��1����X��Y���Ƕ��Ե缫��a�DZ���NaCl��Һ��ʵ�鿪ʼʱ��ͬʱ�����߸����뼸�η�̪��Һ����
�ٵ�����X���ϵĵ缫��ӦʽΪ ����X�������۲쵽��ʵ�������� ��
��Y�缫�ϵĵ缫��ӦʽΪ ������õ缫��Ӧ����ķ����� ��
��2����Ҫ�õ�ⷽ��������ͭ�����Һaѡ��CuSO4��Һ����
��X�缫�IJ����� ���缫��ӦΪ ��
��Y�缫�IJ����� ���缫��ӦʽΪ ��
��˵�������ʷ����ĵ缫��Ӧ����д����
��1����2H++2e-��H2�� �ų����壬��Һ���
��2Cl��2e-=Cl2�� ��ʪ��ĵ⻯�ص�����ֽ����Y�缫��������ֽ����ɫ��
��2���ٴ�ͭ Cu2++2e-=Cu �ڴ�ͭ Cu��2e-=Cu2+
���������������1����X�缫���Դ�ĸ�������������������Һ�е������ӷŵ磬�缫��Ӧʽ��2H++2e-��H2����������Һ�������ӷŵ磬�ƻ���������Χˮ�ĵ���ƽ�⣬������Һ��OH��Ũ��������Һ������ǿ������X�������۲쵽��ʵ�������Ƿų����壬��Һ��졣
��Y�缫����������Һ�е������ӷŵ磬�缫��Ӧʽ��2Cl��2e-=Cl2������������ǿ�����ԣ��ݴ˿��Խ��м��飬���巽���ǰ�ʪ��ĵ⻯�ص�����ֽ����Y�缫��������ֽ����ɫ��
��2����ͭ����ʱ����ͭ�������͵�Դ����������������������Ӧ����ͭ���������͵�Դ�ĸ�����������Һ�е�ͭ���ӷŵ磬������ԭ��Ӧ��
���㣺�����ⱥ��ʳ��ˮ�Լ���ͭ�������й��жϺ͵缫��Ӧʽ����д
�����������Ǹ߿��ж�����ͺ���Ҫ�Ŀ��㣬���ڻ���������Ŀ��飬�ѶȲ�����Ĺؼ�����ȷ���ԭ�����Լ���Һ�����ӵķŵ�˳������������ѧ����Ӧ�������淶�Ĵ������������ѧ��������û���֪ʶ���ʵ�������������

 ��1����ʵ֤��������Ƴ�ԭ��صķ�Ӧͨ���Ƿ��ȷ�Ӧ�����л�ѧ��Ӧ�������Ͽ�����Ƴ�ԭ��ص���
��1����ʵ֤��������Ƴ�ԭ��صķ�Ӧͨ���Ƿ��ȷ�Ӧ�����л�ѧ��Ӧ�������Ͽ�����Ƴ�ԭ��ص���
 ���ԭ���ڻ�ѧ��ҵ���й㷺Ӧ�ã���ͼ��ʾһ�����أ�װ�е��Һc��A��B������缫�壬ͨ��������ֱ����Դ��������ش��������⣺
���ԭ���ڻ�ѧ��ҵ���й㷺Ӧ�ã���ͼ��ʾһ�����أ�װ�е��Һc��A��B������缫�壬ͨ��������ֱ����Դ��������ش��������⣺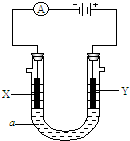 ��I��Li-SOCl2��ؿ����������������õ�صĵ缫���Ϸֱ�Ϊ﮺�̼�����Һ��LiAlCl4-SOCl2����ص��ܷ�Ӧ�ɱ�ʾΪ��4Li+2SOCl2=4LiCl+S+SO2��
��I��Li-SOCl2��ؿ����������������õ�صĵ缫���Ϸֱ�Ϊ﮺�̼�����Һ��LiAlCl4-SOCl2����ص��ܷ�Ӧ�ɱ�ʾΪ��4Li+2SOCl2=4LiCl+S+SO2�� ���ԭ���ڻ�ѧ��ҵ���й㷺Ӧ�ã���ͼ��ʾһ�����أ�װ�е��Һa��X��Y������缫�壬ͨ��������ֱ����Դ������
���ԭ���ڻ�ѧ��ҵ���й㷺Ӧ�ã���ͼ��ʾһ�����أ�װ�е��Һa��X��Y������缫�壬ͨ��������ֱ����Դ������