��Ŀ����
����Ŀ����һ��������þ��ͭ�Ͻ���뵽ϡ������Һ�У�����ǡ����ȫ��Ӧ��������NO����4.48L(��״��)����������Һ�м������ʵ���Ũ��Ϊ3mol/L��NaOH��Һ��������ȫ���������й������в���ȷ����
A.��ʼ����Ͻ�����ʵ���֮��Ϊ0.3mol
B.���ɳ�����������ԭ�Ͻ����������10.2g
C.������ȫʱ����NaOH��Һ�����Ϊ200mL
D.��Ӧ�б���ԭ��δ����ԭ���������ʵ���֮��Ϊ3:1
���𰸡�D
��������
A����״����4.48LNO�����ʵ���Ϊ![]() =0.2mol����HNO3����0.2molNO�õ����ӵ����ʵ���Ϊ��0.2mol��(5-2)=0.6mol��ͭ��þ����2�۽��������ݵ����غ㣬�μӷ�Ӧ�Ľ��������ʵ���Ϊ��
=0.2mol����HNO3����0.2molNO�õ����ӵ����ʵ���Ϊ��0.2mol��(5-2)=0.6mol��ͭ��þ����2�۽��������ݵ����غ㣬�μӷ�Ӧ�Ľ��������ʵ���Ϊ��![]() =0.3mol����A��ȷ��
=0.3mol����A��ȷ��
B��þ��ͭ�Ͻ���Mg(OH)2����Cu(OH)2�����������������ӵ�����Ϊ���������ӵ����������ݵ���غ��֪0.3molMg2+��Cu2+���ɳ���������0.6mol�������ƣ��������������ӵ�����Ϊ��17g/mol��0.6mol=10.2g���������ɳ�����������ԭ�Ͻ����������10.2g����B��ȷ��
C������û��ʣ�࣬���Ժ�Mg2+��Cu2+��Ӧ��NaOH�����ĵ�NaOH��Ϊ0.6mol������NaOH��Һ�����Ϊ![]() =0.2L=200mL����C��ȷ��
=0.2L=200mL����C��ȷ��
D������3Mg+8HNO3(ϡ)=3Mg(NO3)2+2NO��+4H2O��3Cu+8HNO3(ϡ)=3Cu(NO3)2+2NO��+4H2O������Ӧ��֪������ԭ��������δ����ԭ����������ʵ���֮��Ϊ��2��6=1��3����D����
����������ΪD��

����Ŀ���л���A������C��H��O����Ԫ�أ����������Ƿ��͵õ���Ҳ�ɴ���ţ������ȡ��������AΪ��ɫճ��Һ�壬������ˮ��Ϊ�о�A�������ṹ������������ʵ�飺
��ѡ�Լ�������ˮ��2 mol��L��1������Һ��2 mol��L��1NaOH��Һ��Ũ���ᡢNaHCO3��ĩ������Na����ˮ�Ҵ�
ʵ�鲽�� | ʵ����� |
��1��A������ͼ���£� | ��1��֤��A����Է�������Ϊ��__________�� |
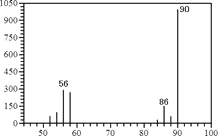
��2������9.0 g A��������O2���ȼ�գ���ʹ��������λ���ͨ��Ũ���ᡢ��ʯ�ң����ֱַ�����5.4 g��13.2 g�� | ��2��֤��A�ķ���ʽΪ�� ________________�� |
��3����ȡ����9.0 g A�����ڲ�ͬ���Թ��С�������һ��A�м���������NaHCO3��ĩ��ַ�Ӧ������_______ L CO2����״������ ����һ��A�м��������Ľ����Ƴ�ַ�Ӧ������________________________ L H2����״������ | ��3��֤��A�ķ����к���һ���Ȼ���һ���ǻ��� |
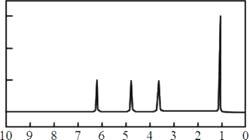
��4��A�ĺ˴Ź�����������ͼ�� | ��4��A�Ľṹ��ʽΪ�� __________________�� |