题目内容
某温度下,体积和pH都相同的盐酸和AlCl3溶液加水稀释时的pH变化曲线如图,下列有关说法正确的是( )
| A.Al(OH)3的电离方程式为:Al(OH)3=Al3++3OH- |
| B.a点溶液中有: c(H+)+c(Al3+)=c(OH-) +3c(Cl-) |
| C.曲线X表示盐酸稀释过程的pH变化 |
| D.b、c两溶液c(OH-)及c(Cl-)均相等 |
C
解析试题分析:A. Al(OH)3是弱电解质。在溶液中存在电离平衡。所以其的电离方程式为:Al(OH)3 Al3++3OH-。错误。B.在任何溶液中都存在电荷守恒。所以在a点溶液中有: c(H+)+3c(Al3+)=c(OH-) +c(Cl-)。错误。C. HCl是强酸,电离产生H+使溶液显酸性,在溶液中不存在电解质的电离平衡。而AlCl3是强酸弱碱盐,水解使溶液显酸性。在水溶液中存在水解平衡。当加水稀释时,强酸的溶液的pH变化较大,盐溶液的pH变化较小。所以曲线X表示盐酸稀释过程的pH变化。正确。D.b、c两点pH相同,则两溶液c(OH-)相同。而c(Cl-)HCl的小于AlCl3的。错误。
Al3++3OH-。错误。B.在任何溶液中都存在电荷守恒。所以在a点溶液中有: c(H+)+3c(Al3+)=c(OH-) +c(Cl-)。错误。C. HCl是强酸,电离产生H+使溶液显酸性,在溶液中不存在电解质的电离平衡。而AlCl3是强酸弱碱盐,水解使溶液显酸性。在水溶液中存在水解平衡。当加水稀释时,强酸的溶液的pH变化较大,盐溶液的pH变化较小。所以曲线X表示盐酸稀释过程的pH变化。正确。D.b、c两点pH相同,则两溶液c(OH-)相同。而c(Cl-)HCl的小于AlCl3的。错误。
考点:考查酸、碱、盐溶液中离子浓度的关系及电解质的电离的知识。

 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案硫化汞(HgS)难溶于水,在自然界中呈红褐色,常用于油画颜料、印泥及朱红雕刻漆器等。某温度时,HgS在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
| A.向硫化汞的浊液中加入硫化钠溶液,硫化汞的Ksp减小 |
| B.图中a点对应的是饱和溶液 |
| C.向c点的溶液中加入Hg(NO3)2,则c(S2-)减小 |
| D.升高温度可以实现c点到b点的转化 |
部分弱酸的电离平衡常数如下表:
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | K=1.77×10-4 | K=4.9×10-10 | K1=4.2×10-7 K2=5.6×10-11 |
下列说法正确的是
A.CN- + H2O + CO2 =" HCN" + HCO3-
B.0.1mol·L-1HCOONa溶液比0.1mol·L-1NaCN溶液的pH大
C.用0.1mol·L-1NaOH溶液中和等浓度的HCN和HCOOH时前者所需NaOH溶液体积大
D.0.1mol·L-1NaHCO3溶液中粒子浓度的大小:c(Na+)> c(HCO3-)>c(H+)>c(OH-)
已知难溶性物质K2SO4·MgSO4·2CaSO4在水中存在如下平衡:
K2SO4·MgSO4·2CaSO4(s)=2Ca2++2K++Mg2++4SO42-,不同温度下,K+的浸出浓度与溶浸时间的关系如右图所示,则下列说法错误的是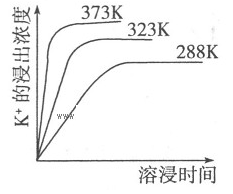
| A.向该体系中加入饱和NaOH溶液,溶解平衡向右移动 |
| B.向该体系中加入饱和碳酸钠溶液,溶解平衡向右移动 |
| C.该平衡的Ksp=c(Ca2+)·c(K+)·c(Mg2+)·c(SO42-) |
| D.升高温度,反应速率增大,平衡向正反应方向移动 |
某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是
| A.加入Na2SO4可使溶液由a点变到b点 |
| B.通过蒸发可以使溶液由d点变到c点 |
| C.b点有BaSO4沉淀生成 |
| D.a点对应的Ksp大于c点对应的Ksp |
海水中含有丰富的镁资源。某同学设计了从模拟海水中制备MgO的实验方案:
注:溶液中某种离子的浓度小于1.0×10-5 mol/L,可认为该离子不存在;实验过程中,假设溶液体积不变。已知:KSp(CaCO3)=4.96×10-9;KSp(MgCO3)=6.82×10-6;KSp[Ca(OH)2]=4.68×10-6;KSp[Mg(OH)2]="5.61×10" -12。
下列说法不正确的是
| A.沉淀物X为CaCO3 |
| B.滤液M中存在Mg2+和Ca2+ |
| C.滤液N中存在Mg2+、Ca2+ |
| D.步骤②中若改为加入4.2 g NaOH固体,沉淀物Y只有Mg(OH)2 |
向10 mL 0.1 mol·L-1 NaOH溶液中逐滴加入0.1 mol·L-1的CH3COOH溶液,其pH逐渐减小,图中a,b,c三点的pH为实验中所测得,下列有关说法中一定正确的是( )
| A.当7<pH<13时,溶液中c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| B.当pH=7时,所加CH3COOH溶液的体积为10 mL |
| C.当5<pH<7时,溶液中c(CH3COO-)>c(Na+) |
| D.继续滴加0.1 mol·L-1的CH3COOH溶液,溶液的pH最终可以变化至1 |
室温下,对于0.10 mol·L-1的氨水,下列判断正确的是( )
| A.与AlCl3溶液发生反应的离子方程式为Al3++3OH-=Al(OH)3↓ |
| B.加水稀释后,溶液中c(NH4+)·c(OH-)变大 |
| C.用HNO3溶液完全中和后,溶液不显中性 |
| D.其溶液的pH=13 |