题目内容
2.某混合气体X,可能由H2、CO、CO2和水蒸气中的一种或几种组成,现将混合气体通入足量灼热的CuO,完全反应后,固体CuO质量减少1.6g;再将反应后的混合气体全部导入足量的澄清石灰水中,生成白色沉淀10g.根据以上信息,分析下列有关X的组成推断正确的是( )| A. | X一定只由CO组成 | |
| B. | X一定只由H2和CO2组成 | |
| C. | X可能由0.1 g H2和4.4 g CO2组成 | |
| D. | X可能由0.1 g H2、1.4 g CO和2.2 g CO2组成 |
分析 将反应后的气体全部通入过量的澄清石灰水中,充分反应后得到10g白色沉淀为碳酸钙,其物质的量为$\frac{10g}{100g/mol}$=0.1mol,根据碳元素守恒可知,混合气体通过灼热的CuO后二氧化碳的质量为0.1mol×44g/mol=4.4g.固体质量减少1.6g,至少含有H2、CO一种,若为CO,发生反应CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2,需要CO质量为2.8g、生成CO2为4.4g;若为H2,发生反应H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O,需要氢气质量为0.2g,没有CO2生成,故混合气体不能只有H2、CO组成.若不含CO,则一定含有H2、CO2,若不含H2,则一定含有CO、不含CO2,若含有H2、CO,则一定含有CO2,据此解答.
解答 解:将反应后的气体全部通入过量的澄清石灰水中,充分反应后得到10g白色沉淀为碳酸钙,其物质的量为$\frac{10g}{100g/mol}$=0.1mol,根据碳元素守恒可知,混合气体通过灼热的CuO后二氧化碳的质量为0.1mol×44g/mol=4.4g.固体质量减少1.6g,至少含有H2、CO一种,
若为CO,则:CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2 固体质量减少△m
28g 44 16g
m(CO) m(CO2) 1.6g
所以,m(CO)=$\frac{2.8g×1.6g}{16g}$=2.8g,m(CO2)=$\frac{44g×1.6g}{16g}$=4.4g,生成二氧化碳的质量等于混合气体通过灼热的CuO后二氧化碳的质量,
若为H2,则:H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O 固体质量减少△m
2g 16g
m(H2) 1.6g
所以,m(H2)=$\frac{2g×1.6g}{16g}$=0.2g,没有CO2生成,
故混合气体不能只有H2、CO组成,若不含CO,则一定含有H2、CO2,若不含H2,则一定含有CO、不含CO2,若含有H2、CO,则一定含有CO2,
A.由上述分析可知,X可能只有CO,也可能为H2、CO2等组成,故A错误;
B.由上述分析可知,X不一定只由H2和CO2组成,故B错误;
C.由上述分析可知,X若由H2和 CO2组成,氢气为0.2g,二氧化碳为4.4g,故C错误;
D.0.1g H2反应,使CuO固体质量减少1.6g×$\frac{0.1g}{0.2g}$=0.8g,1.4g CO反应,使CuO固体质量减少1.6g×$\frac{1.4g}{2.8g}$=0.8g,固体共减少1.6g,生成CO2为4.4g×$\frac{1.4g}{2.8g}$=2.2g,混合气体通过灼热的CuO后二氧化碳的质量为2.2g+2.2g=4.4g,故X可能由0.1g H2,1.4g CO,2.2g CO2组成,故D正确,
故选D.
点评 本题考查混合物的有关计算、物质组成的推断等,关键是根据二氧化碳的质量判断可能的组成,难度中等.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 酸性:HClO4>HBrO4>HIO4 | B. | 碱性:NaOH>Mg(OH)2>Al(OH)3 | ||
| C. | 酸性:HCl>HBr>HI | D. | 非金属性:F>O>S |
| A. | 将等物质的量的甲烷与氯气充分反应生成物中物质的量最大的是CH3Cl | |
| B. | 苯乙烯生成乙基环己烷不属于取代反应 | |
| C. | 乙烯与溴的四氯化碳溶液反应生成1,2-二溴乙烷 | |
| D. | 煤的干馏、石油裂化和乙烯聚合均属于化学变化 |
| A. | $\frac{56m}{V}$mol•L-1 | B. | $\frac{3m}{56V}$mol•L-1 | C. | $\frac{m}{56V}$mol•L-1 | D. | $\frac{3m}{112V}$mol•L-1 |
| A. | 3种 | B. | 8种 | C. | 10种 | D. | 12种 |
| A. | 食用蔬菜、水果可补充维生素 | |
| B. | 适当补充钙元素可以预防甲状腺肿大 | |
| C. | 熟石灰可用于改良酸性土壤 | |
| D. | 生活污水处理后排放有利于保护环境 |
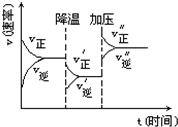 如图是可逆反应A+2B?2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断( )
如图是可逆反应A+2B?2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断( )| A. | 若A、B是气体,则D是液体或固体 | B. | A、B、C、D均为气体 | ||
| C. | 逆反应是放热反应 | D. | 达平衡后,v(A)正=2 v(C)逆 |
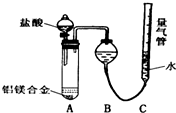 铝镁合金已成为轮船制造、化工生产等行业的重要材料.研究性学习小组的三位同学,为测定已知质量的铝镁合金(设不含其它元素)中镁的质量分数,设计下列三种不同实验方案(所加试剂均为足量)进行探究.填写下列空白.
铝镁合金已成为轮船制造、化工生产等行业的重要材料.研究性学习小组的三位同学,为测定已知质量的铝镁合金(设不含其它元素)中镁的质量分数,设计下列三种不同实验方案(所加试剂均为足量)进行探究.填写下列空白.